电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。
2、用电导法测量醋酸在水溶液中的解离平衡常数。
3、掌握恒温水槽及电导率仪的使用方法。
二、实验原理
1、电导G可表示为: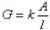 (1)
(1)
式中,k为电导率,电极间距离为l,电极面积为A,l/A为电导池常数Kcell,单位为m-1。
本实验是用一种已知电导率值的溶液先求出Kcell,然后把欲测溶液放入该电导池测出其电导值G,根据(1)式求出电导率k。
摩尔电导率与电导率的关系: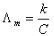 (2)
(2)
式中C为该溶液的浓度,单位为mol·m-3。
2、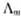 总是随着溶液的浓度降低而增大的。
总是随着溶液的浓度降低而增大的。
对强电解质稀溶液,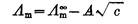 (3)
(3)
式中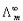 是溶液在无限稀释时的极限摩尔电导率。A为常数,故将
是溶液在无限稀释时的极限摩尔电导率。A为常数,故将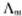 对
对 作图得到的直线外推至C=0处,可求得
作图得到的直线外推至C=0处,可求得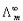 。
。
3、对弱电解质溶液,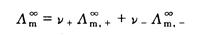 (4)
(4)
式中 、
、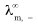 分别表示正、负离子的无限稀释摩尔电导率。
分别表示正、负离子的无限稀释摩尔电导率。
在弱电解质的稀薄溶液中,解离度与摩尔电导率的关系为: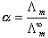 (5)
(5)
对于HAc, (6)
(6)
HAc的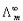 可通过下式求得:
可通过下式求得:
把(4)代入(1)得: 或
或
以C 对
对 作图,其直线的斜率为
作图,其直线的斜率为 ,如知道
,如知道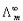 值,就可算出Ko
值,就可算出Ko
三、实验仪器、试剂
仪器:梅特勒326电导率仪1台,电导电极1台,量杯(50ml)2只,移液管(25ml)3只,洗瓶1只,洗耳球1只
试剂:10.00(mol·m-3)KCl溶液,100.0(mol·m-3)HAc溶液,电导水
四、实验步骤
1、打开电导率仪开关,预热5min。
2、KCl溶液电导率测定:
⑴用移液管准确移取10.00(mol·m-3)KCl溶液25.00 ml于洁净、干燥的量杯中,测定其电导率3次,取平均值。
⑵再用移液管准确移取25.00 ml电导水,置于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
⑶用移液管准确移出25.00 ml上述量杯中的溶液,弃去;再准确移入25.00 ml电导水,只于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
⑷重复⑶的步骤2次。
⑸倾去电导池中的KCl溶液,用电导水洗净量杯和电极,量杯放回烘箱,电极用滤纸吸干
3、HAc溶液和电导水的电导率测定:
⑴用移液管准确移入100.0(mol·m-3)HAc溶液25.00 ml,置于洁净、干燥的量杯中,测定其电导率3次,取平均值。
⑵再用移液管移入25.00 ml已恒温的电导水,置于量杯中,搅拌均匀后,测定其电导率3次,取平均值。
⑶用移液管准确移出25.00 ml上述量杯中的溶液,弃去;再移入25.00 ml电导水,搅拌均匀,测定其电导率3次,取平均值。
⑷再用移液管准确移入25.00 ml电导水,置于量杯中,搅拌均匀,测定其电导率3次,取平均值。
⑸倾去电导池中的HAc溶液,用电导水洗净量杯和电极;然后注入电导水,测定电导水的电导率3次,取平均值。
⑹倾去电导池中的电导水,量杯放回烘箱,电极用滤纸吸干,关闭电源。
五、数据记录与处理
1、大气压:102.08kPa 室温:17.5℃ 实验温度:25℃
已知:25℃时10.00(mol·m-3)KCl溶液k=0.1413S·m-1;25℃时无限稀释的HAc水溶液的摩尔电导率=3.907*10-2(S·m2·m-1)
⑴测定KCl溶液的电导率:

⑵测定HAc溶液的电导率:
电导水的电导率k(H2O)/ (S·m-1):7 *10-4S·m-1

2、数据处理
⑴将KCl溶液的各组数据填入下表内:

以KCl溶液的 对
对 作图
作图

根据 ,截距即为
,截距即为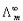 ,得
,得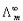 =154*10-4 S·m2·mol-1
=154*10-4 S·m2·mol-1
⑵HAc溶液的各组数据填入下表内:
HAc原始浓度:0.1127 mol·dm-3

k = k’- kH2O
uS.cm-1=10-4S·m-1
CHAc=0.1127 mol·dm-3=112.7 mol·m-3
kH2O =7*10-4S·m-1
k(HAc测量)=560*10-4 S·m-1 k(HAc)= k(HAc测量)- kH2O=553*10-4 S·m-1
Λm=553*10-4/112.7=4.91*10-4 S·m2·mol-1
Λm -1=2.04*103 S-1·m-2·mol C =k=553*10-4 S·m-1
=k=553*10-4 S·m-1
α=4.91*10-4/3.907*10-2=0.0126
Kc=0.1127*0.01262/1*(1-0.0126)=1.81*10-5
以C 对
对 作图应得一直线,直线的斜率为
作图应得一直线,直线的斜率为 ,由此求得Ko,于上述结果进行比较。
,由此求得Ko,于上述结果进行比较。
直线的斜率 =2.87*10-5 所以:Ko=2.87*10-5 /103*(3.907*10-2)2=1.88*10-5
=2.87*10-5 所以:Ko=2.87*10-5 /103*(3.907*10-2)2=1.88*10-5
计算出来的值与画图做出来的相差:(1.88-1.753)*10-5=1.27*10-6

