实验七 曝气设备充氧能力的测定实验
1.实验目的
(1) 握测定曝气设备的KLa和充氧能力α、β的实验方法及计算QS。
(2) 评价充氧设备充氧能力的好坏。
(3) 掌握曝气设备充氧性能的测定方法
2.实验原理
活性污泥处理过程中氧气设备的作用是使氧气、活性污泥、营养物三者充分混合,使污泥处于悬浮状态,促使氧气从气相转移到液相,从液相转移到活性污泥上,保证微生物有足够的氧进行物质代谢。由于氧的供给是保证生化处理过程正常进行的主要因素,因此工程设计人员通常通过实验来评价曝气设备的供氧能力。
在现场用自来水实脸时,先用Na2SO3(或N2)进行脱氧,然后在溶解氧等于或接近零的状况下再曝气,使溶解氧升高趋于饱和水平。假定整个液体是完全混合的,符合一级反应,此时水中溶解氧的变化可以用下式表示:
 (4-6-1)
(4-6-1)
式中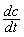 ——氧转移速率,mg/(L·h);
——氧转移速率,mg/(L·h);
KLa——氧的总传递系数,L/h,
CS——实验室的温度和压力下,自来水的溶解氧饱和浓度,mg/L;
C——相应某一时刻t 的溶解氧浓度,mg/L。
将上式积分,得
 (4-6-2)
(4-6-2)
测得CS和相应干每一时刻的C后绘。In(CS-C)与t的关系曲线,或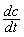 与c的关系曲线便可得到KLa,c= CS- C。
与c的关系曲线便可得到KLa,c= CS- C。
由于溶解氧饱和浓度,温度、污水性质和紊乱程度等因素均影响氧的传递速率,因此应进行温度、压力校正,并测定校正污水性质影响的修正系数α、β。所采用的公式如下:
 (4-6-3)
(4-6-3)
 (4-6-4)
(4-6-4)
 (4-6-5)
(4-6-5)
 (4-6-6)
(4-6-6)
充氧能力为
 (4-6-7)
(4-6-7)
3.实验设备与试剂
(1)溶解氧侧定仪。
(2)空压机。
(3)曝气筒。
(4)搅拌器。
(5)秒表。
(6)分析天平。
(7)烧杯。
(8)亚硫酸钠(Na2SO3·7H2O)。
(9)氧化钻(CoCl2·6H2O)。
(10)试验装置(见图4-6-1)。
4.实验步骤
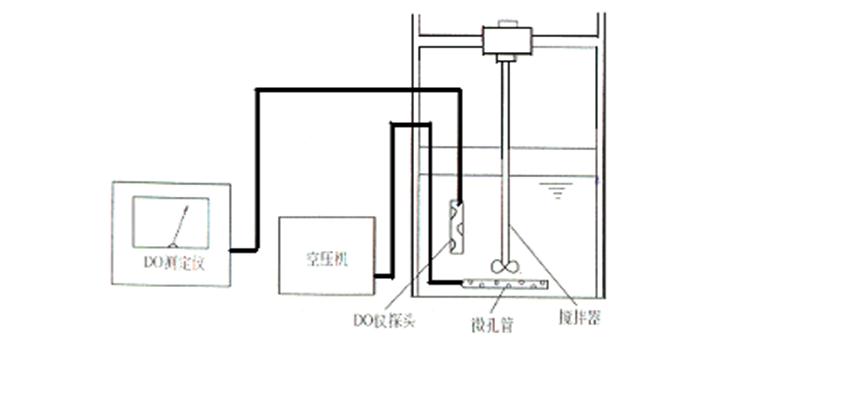 图4-6-l 曝气设备充氧能力实验装置图
图4-6-l 曝气设备充氧能力实验装置图
(1)向曝气筒内注人自来水,测定水样体积V(L)和水温t(℃)。
(2)由水温查出实验条件水样溶解氧饱和值CS,并很据CS和V求投药量,然后投药脱氧。
①脱氧剂亚硫酸钠(Na2SO3·7H2O)的用量计算。在自来水中加人Na2SO3·7H2O还原剂来还原水中的溶解氧
CoCl2

相对分子质量之比为

故Na2SO3·7H2O理论用量为水中溶解氧的16倍,而水中有部分杂质会消耗亚硫酸钠,故实际用量为理论用量的1.5倍。
所以实际投加的Na2SO3·7H2O用量为

式中 W——亚硫酸钠投加量;
CS——实验时水文条件下水中的饱和溶解氧值,mg/L;
V——水样体积,m3。
②根据水样体积V确定催化剂(钴盐)的投加量。
经验证明,清水中有效钴离子浓度约0.4mg/L为好,一般使用氧化钴(CoCl2)。因为

所以单位水样投加钴盐量为
CoCI2·6H2O 0.4x4.0=1.6g/m3
本实验所需投加钴盐为
CoCI2·6H2O 1.6V(g)
式中 V——水祥体积,m3。
③将Na2S03用热水化开,均匀倒人曝气简内,溶解的钻盐倒人水中.并开动搅拌叶轮轻徽搅动使其混合,进行脱氧。
(3)当清水脱氧至零时,提高叶轮转速便进行曝气,并计时。每隔0.5min测定一次溶解氧(用碘量法每隔1min测定一次),直到溶解氧值达到饱和为止。
5.实验结果整理
(1)将测定数据记录于表4-6-1中
水温℃,水样体积m3,CSmg/L,亚硫酸钠用量g,氯化钴用量。
表4-6-1 实验记录

(2)根据测定记录计算KLa值
① 根据公式计算

②用图解法计算KLa值,用半对数坐标纸作亏氧值CS-Ct和时间的关系曲线,其斜
率即为KLa值。
③计算叶轮充氧能力QS

式中 1000——由mg/L转化为kg/m3的系数;
60——由min 转化为h的系数;
KLa——氧的总转移系数,L/min;
CS——饱和溶解氧,mg/L;
V——水样的体积,m3。
④计算污水性质影响的修正系数α、β
 ,
,
6.注意事项
(1)每个实验所用设备、仪器较多,实验前必须熟悉仪器的使用方法及注意事项。
(2)认真调试仪器设备,特别是溶解氧测定仪,要定时更换探头内溶解液,使用前标定零点及满度。
(3)严格控制各项基本实验条件,如水温、搅拌强度等,尤其是对比实验更应严格控制。
(4)所加试剂应溶解后,再均匀加入曝气简内。
7.思考题
(1)氧总转移系数KLa的意义是什么,怎样计算?
(2)曝气设各充氧性能指标为何均是清水?
(3)鼓风曝气设备与机械曝气设备充氧性能指标有何不同?
(4)α、β值的测定有何惫义?影响α、β的因素有哪些?
(5)注意实验中出现的异常情况,分析具原因。
第二篇:实验八 表面曝气充氧实验 2

水污染控制工程实验
实验报告
姓 名:
专业年级: 试验日期:
环境科学与工程学院
中国海洋大学
实验八 表面曝气充氧实验
一、 实验目的
通过实验了解空气扩散过程中氧的转移规律,以及确定该表曝器的总转移系数Kla值。
二、 实验原理
曝气的作用是向液相供给溶解氧。氧由气相转入液相的机理常用双膜理论来解释。双膜理论是基于在气液两相界面存在着两层膜(气膜和液膜)的物理模型。氧在膜内总是以分子扩散方式转移的,其速度总是慢于在混合液内发生的对流扩散方式的转移。所以只要液体内氧未饱和,则氧分子总会从气相转移到液相的。
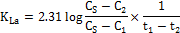
Cs —液相氧的饱和浓度(kgO2/m3)
C1、C2—在t1、t2 时所测得的溶解氧浓度
清水(在现场用自来水)一般含有溶解氧,通过加入无水亚硫酸钠(或氮气)在氯化钴的催化作用下,能够把水体中的溶解氧消耗掉,使水中溶解氧降到零,其反应式为:
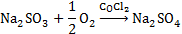
通过使用空气压缩机或充氧泵把空气中的氧气打入水体,使水体系的溶解氧逐渐提高,直至溶解氧升高到接近饱和水平。
三、实验设备及药剂
1、模型曝气池(桶或玻璃缸);
2、空气压缩机或充氧泵; 3、秒表;
4、1L 量筒、长玻棒、虹吸管;
5、无水亚硫酸钠; 6、氯化钴;
7、溶解氧测定装置(DO测定仪或碘量法测定DO所需的仪器试剂)
四、实验步骤
1、将水箱洗净放自来水至指定的叶轮浸没设定深度处,计算水的体积。
2、用溶解氧探测仪测量水样中的溶解氧和温度。
3、投加亚硫酸钠和氯化钴分别溶解后进行脱氧,投加亚硫酸钠按每1mg/L 的溶解氧需投加9mg/L,计算亚硫酸钠的数量。
4、将亚硫酸钠和约1g 的氯化钴分别溶解后投入水箱,打开搅拌器,经1~2min,即把溶解氧脱掉。
5、把充氧装置的探头放入曝气池内开始曝气,计时,在稳定曝气的条件下,每隔一段时间(根据溶解氧的变化大小来去顶)测定一次水中的溶解氧,并作记录,曝气至溶解氧不再明显增长为止(达到近似饱和)。
五、实验数据记录
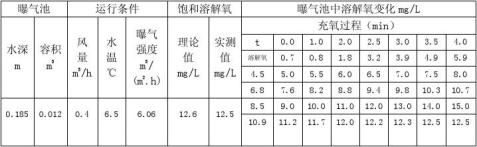
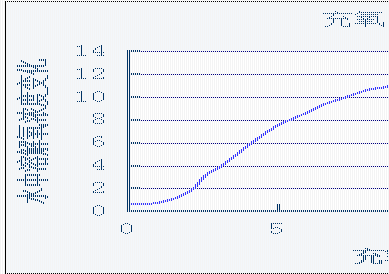
1、以充氧时间t为横坐标,水中溶解氧浓度变化为纵坐标作图绘制充氧曲线,
任取两点;[A点坐标为(t1,C1),B点坐标(t2,C2)],计算KLa。
取A点坐标(3,3.9),B点坐标(6,8.8)
KLa?2.3?lg
CS?C1112.6?3.91
??2.3?lg??0.28min?1
CS?C2t2?t112.6?8.83
2、以充氧时间t为横坐标,log上求出KLa。
3、分别计算充氧量,氧利用系数。
CS?C1
为纵坐标作图,从其支线的斜率
CS?C2
转移到一定体积清水中的总氧量
QS?KLa?CS?V?0.28??12.6?0.012?1000?42.336mg
供氧量S?0.28?GS?860.677mg QS42.336??0.049 S860.677氧利用效率EA?
七、实验心得
1、 由实验结果得到溶解氧在前10分钟浓度迅速增加,之后溶解氧浓度不再增加,这是因为当混合液中的氧的浓度较低时,由于具有最大的推动力,因此氧的转移率最大。
2、 实验的精度的关键是溶解氧的固定与各种药剂的加量、滴定硫代硫酸钠的用量。滴定过程中要边滴定边摇晃,而且滴定速度不能太快,要准确地捉住滴定终点。

