液 质 联 用 分 析
一、实验目的
1.了解液相色谱仪和质谱仪的原理、基本构造。
2.学会运用液质联用仪检测样品,会选择合适的质谱电离源检测样品,会运用色谱对混合物中的目标物分离和定量。
3.了解、熟悉质谱基本操作技术及质谱检测器的基本组成及功能原理。
二、实验原理
色谱分析是运用物种在固定相和流动相两相间的分配系数不同而达到分离的效果的一种分离技术,主要目的是对混合物中目标产物进行分离和定量的一种分析技术。质谱是通过测定样品的质荷比来进行分析的一种方法。通过液-质谱联用(LC-MS)技术可实现样品的分离和定量分析,达到快速灵敏的效果。
(1)液质联用系统的常见部件
HPLC(色谱分离)→ 接口(样品引入)→ 离子源(离子化)→ 分析器 → 检测器(离子检测)→ 数据处理(数据采集及控制)→ 色谱图;
质谱仪器构成:包括真空系统、电喷雾离子源、质量分析器及检测器。
三、仪器与试剂
Waters ZQ液质联用仪(LC/MS)
甲醇溶液、苯甲酸、十六烷基三甲基溴化铵
四、实验内容
运用液相色谱-质谱联用仪测定苯甲酸和十六烷基溴化铵(CTAB)的质荷比,熟悉仪器的操作流程,并能从所得的质谱图中指认出相应物质对应的质荷比,能对谱图做定性的描述。
五、实验步骤
1.打开仪器开关和计算机电源。
2.待仪器运转正常,打开测试软件,先用甲醇清洗柱子(在Load状态下进样,分析时在Inject状态下);
3.选择分析模式(正、负离子模式),输入分析的样品名;
4.利用软件进行数据分析。
五、实验结果与分析
(1)CTAB(正离子模式)

CTAB:正离子模式时在 处有强的信号峰,为
处有强的信号峰,为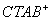 。
。
(2)CTAB(负离子模式)

CTAB:负离子模式时在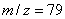 和
和 处有强的信号峰,且强度为1:1,可以判断为
处有强的信号峰,且强度为1:1,可以判断为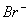 。
。
说明十六烷基三甲基溴化胺用两种模式都可以。
(3)苯甲酸(负离子模式)

苯甲酸:负离子模式时在 处有强信号峰,为苯甲酸根离子;正离子模式时有很多杂质峰,说明苯甲酸适用负离子模式。
处有强信号峰,为苯甲酸根离子;正离子模式时有很多杂质峰,说明苯甲酸适用负离子模式。
第二篇:食品分析实验报告

食品分析实验报告
姓名:李治友
学号:2010040618
指导老师:王振伟
班级:食品1001班
系别:环境与化学工程系
项目一:全脂乳粉中水分含量的测定
一、目的要求
1.学习和领会常压干燥法测定水分的原理及操作要点。
2.乳粉中水分含量的高低直接影响乳粉质量及保藏性(2.1%左右为宜),掌握好其测定方法对以后从事相关行业必定会打下坚实的基础。
二、实验原理
食品中的水分受热以后,产生的蒸汽气压高于在电热干燥箱中的空气分压,从而使水分蒸发出来。同时由于不断地供给热量及不断蒸发出水分二达到完全干燥的目的。食品干燥的速度取决于这个压差的大小。
食品中的水分一般指在100℃±5℃直接干燥的情况下所失去物质的总重。此法办法适用于95~105℃下,不含或含其他挥发性物质甚微的食品
三、实验仪器
称量瓶,干燥器,恒温干燥箱。
四:实验步骤
1.取洁净的玻璃扁形称量瓶,置于105℃的干燥箱中,瓶盖倾斜于瓶边,加热30分钟,取出,盖好,置于干燥器中冷却30分钟,称量其重量。
2.称取2.00~3.00克奶粉样品于称量瓶中,加盖,精密称量后放于105℃干燥箱中,瓶盖倾斜于瓶边,干燥2~4h后,盖好盖取出,放入干燥箱中冷却30分钟后称量。
3.再放入100℃±5℃干燥箱中干燥30分钟,取出,放入干燥器中冷却30分钟再称量,重复以上步骤,直至前后两次的质量之差不超过2毫克,即为恒重。
五:结果处理
1.数据记录

2.结果计算
X=(M2-M3)/(M1-M3)×100
=(22.1906-20.1917)/(22.4117-20.1917)×100
=9.004g/100g
其中M2=22.1906代表恒重后称量瓶和样品总重,M3=20.1917代表称量瓶重,M1=22.4117代表称量前称量瓶和样品总重。
六:注意事项
要充分的干燥称重,直至前后质量之差小于2毫克,否则继续进行干燥,且要保证干燥后的样品不能再次吸收水分。
七:实验感受
此方法简单,易操作,结果准确,因此掌握好此方法对学习食品专业的我们来说至关重要。
项目二:面粉中灰分含量的测定
一、目的要求
1. 学习和了解直接灰化法测定灰分的原理及操作要点。
2. 掌握面粉中灰分测定的方法和操作技能。
二、实验原理
一定质量的食品在高温下经灼烧后,去除了有机物所残留的无机物称为灰分。样品质量发生了改变,根据样品的失重,即可计算出总会分的含量。
三:实验仪器
高温电炉,瓷坩埚,坩埚钳,电子天平,干燥箱。
四:实验步骤:
1.取洁净的石英坩埚置于高温电炉中,置于575℃下灼烧30分钟,冷却至200℃以下后取出,放入干燥器中冷却至室温,精密称量,并重复灼烧至恒重。
2.加入2至3克样品放于其中,准确称量。
3.样品先以小火加热是样品充分炭化至无烟,然后置于高温电炉中,在575℃灼烧4小时。冷却200℃以下后取出放入干燥器中冷却30分钟,若没有灰化完全,可重复以上步骤至称量前后质量之差不超过0.5毫克,即为恒重。
五:结果处理
1.数据记录

2.结果计算
X=(M3-M1)/(M2-M1)×100
=(31.6073-31.5970)/( 33.7401-31.5970)×100
=4.8061g/100g
其中M3=31.6073代表恒重后称量瓶和样品总重,M1=31.5970代表称量瓶重,M2=33.7401代表称量前称量瓶和样品总重。
六:注意事项
在把药品放入高温电炉前或者是从电炉中取出药品,都要事先在炉口出进行预热和预冷,以防止温差过大而导致坩埚炸裂,毁坏仪器,另外电炉温度极高,一定要做好防护工作。
七:实验感受
此方法简单,易操作,结果准确,因此掌握好此方法对学习食品专业的我们来说至关重要,因此掌握好此方法对学习食品专业的我们来说至关重要。
项目三:酱油中氨基酸态氮含量的测定
一、目的要求
1.理解电位滴定法测氨基酸态氮的测定。
2.掌握电位滴定法测定氨基酸态氮的方法及操作要点。
二、实验原理
氨基酸含有羟基和氨基,利用氨基酸的两性作用,加入甲醛固定氨基的碱性,使羧基显示出酸性,用氢氧化钠标准溶液滴定后进行定量,以酸度计测定终点。
三:实验仪器与试剂
酸度计,磁力搅拌器,滴定管,36%甲醛溶液,0.05moL/L氢氧化钠标准溶液。
四:实验步骤
1.准确吸取酱油5毫升,置于100毫升容量瓶中,加水至刻度混匀后吸取20毫升,置于200毫升烧杯中,加水60毫升,插入酸度计,开动磁力搅拌器,用氢氧化钠标准溶液滴定至酸度计指示PH=8.2,记录用去氢氧化钠标准溶液的体积。
2.向上述溶液中加入甲醛溶液10毫升,混匀,继续用氢氧化钠标准溶液滴定至PH=9.2,记录用去氢氧化钠标准溶液的体积。
3.取水80毫升,先用氢氧化钠标准溶液滴定至PH=8.2,记录用去氢氧化钠标准溶液的体积,再加入10毫升甲醛溶液,继续用氢氧化钠标准溶液滴定至PH=9.2,记录用去氢氧化钠标准溶液的体积。
五:实验结果
X=(V1-V2)×C×0.014×10000÷(5×V3)
=(9.08-3.86) ×0.05×0.014×10000÷(5×20)
=0.3654g/100Ml
其中V1=9.08代表测定用的样品稀释后加入甲醛后消耗的氢氧化钠溶液的体积,V2=3.86代表空白样稀释后加入甲醛后消耗的氢氧化钠溶液的体积,V3=20代表吸取稀释液用去量。
六:实验感受
此方法简单,易操作,结果准确,应该是我们专业必须要掌握的一种方法,这样才能为将来从事相关专业打下一个良好的基础。
项目四:啤酒中双乙酰的测定
一:目的要求
双乙酰赋予啤酒特殊的风味,是品评啤酒成熟与否的主要依据。含量的多少直接影响着啤酒的品质。
二:实验试剂
1%邻苯二胺溶液,4N盐酸溶液,消泡剂
三:实验步骤
1、蒸馏:在25ml量筒内加约2.5ml水,置于冷凝器下端,使冷凝器下端浸入水中。量取未除去气的啤酒100ml,加入2—4滴消泡剂(没有的话也可不加)。迅速加入到已预先加热好的蒸馏器中,继续加热,蒸馏至馏出液近25ml,取下量筒,用水定容至25ml混匀。
2、显色:分别取10ml馏出液置于试管中,第一支试管中加入0.5ml1%的邻苯二胺溶液,第二支试管中不加(作空白参考),充分摇匀,置暗处理反应20~ 30分钟,第一支试管中加入2ml4N盐酸溶液,第二支试管中加入2.5ml4N盐酸溶液混匀。
3、比色:在335纳米波长下,2cm的比色皿,用紫外分光光度计测出样品和空白的光密度,比色操作需在20分钟内完成。
四:数据处理
双乙酰(mg/l)=E335×1.2-0.01
式中:E335——样品光密度与空白光密度之差
1.2——校正系数(多次用纯双乙酰测得经验数据)
0.01——补正数
五:结果计算
双乙酰(mg/l)=0.44×1.2-0.01=0.518
六:注意事项
该实验需要蒸馏仪器,而仪器在组装时尤其要注意细节,否则很可能造成仪器的损坏,所以要注意蒸馏装置的安装和固定。
项目五:总糖含量的测定
一:目的要求
碳水化合物的测定在食品工业中具有特别重要的意义。在食品加工工艺中,糖类对食品的形态、组织结构、理化性质及其色、香、味等具有很大的影响,同时糖类的含量还是食品营养价值高低的重要标志,也是某些食品重要的质量指标。碳水化合物的测定是食品的主要分析项目之一。
二、实验原理
样品经处理出去蛋白质等杂质后,加入稀盐酸在加热条件下是蔗糖水解转化为还原糖,再以直接滴定法滴定水解后样品中还原糖的总量。
三:实验试剂:
(1)盐酸:6mol/l。
(2)甲基红指示剂:1g/L,称取0.1g甲基红,用体积分数60%的乙醇溶解并定容到100ml。
(3)氢氧化钠溶液:200g/L。
(4)碱性酒石酸铜甲液:称取15g硫酸铜(CuSO4.5H2O)及0.05g亚甲基蓝,溶于水中并稀释至1000ml。
(5)碱性酒石酸铜乙液:称取50g酒石酸钠钾及75g氢氧化钠,溶于水中,再加入4g亚铁氰化钾,完全溶解后,用水稀释至1000ml,贮存于橡胶塞玻璃瓶内。
(6)乙酸锌溶液:称取21.9g乙酸锌【Zn(CH3Coo)2.2H2O】,加3ml冰醋酸,加水溶解并稀释至1000ml。
(7)106g/L亚铁氰化钾溶液:称取10.6g亚铁氰化钾【K4Fe(CN)6.3H2O】,溶于水中,稀释至100ml。
(8)浓盐酸
(9)1g/L葡萄糖标准溶液:准确称取1.000g98~100℃烘干至恒重的无水葡萄糖,加水溶解后,加入5ml盐酸(防止微生物生长),转移入1000ml容量瓶中,并用水稀释至刻度。
四:实验步骤
1、样品处理:称取2.50~5.00g固体样品或吸取25.00~50.00ml液体样品至于250ml容量瓶中,加水50ml摇匀后慢慢加入5ml醋酸锌及5ml亚铁氰化钾溶液,加水至刻度,混匀,静置30分钟。干虑,弃去粗滤液,收集滤液备用。
2、碱性酒石酸铜溶液的标定,准确吸取碱性酒石酸铜甲液和乙液各5毫升,置于250毫升的锥形瓶中,加水10毫升,加入2粒玻璃珠。从滴定管中加约9毫升葡萄糖标准溶液,加热使其在2分钟内沸腾,趁热继续用葡萄糖标准溶液滴定,直至蓝色刚好褪去即为终点,记录所消耗的葡萄糖标准溶液,平行做三次,算出平均值。计算每10毫升碱性酒石酸钠溶液,相当于葡萄糖的质量:
A=VC
其中:C代表葡萄糖标准溶液的浓度,mg/mL
V代表滴定时所消耗的葡萄糖标准溶液的体积,Ml。
A代表10毫升碱性酒石酸铜溶液相当于葡萄糖的质量,mg。
3.样品的预测定,准确吸取碱性酒石酸铜甲液和乙液各5毫升,置于250毫升的锥形瓶中,加水10毫升,加入2粒玻璃珠,加热使其在2分钟内沸腾,趁热以先快后满的速度滴入样液,滴定时必须始终保持沸腾。待溶液颜色变浅时,以每2秒1滴的速度继续加入,直至蓝色刚好褪去即为终点,记录所消耗的葡萄糖标准溶液。
4. 样品的测定,准确吸取碱性酒石酸铜甲液和乙液各5毫升,置于250毫升的锥形瓶中,加水10毫升,加入2粒玻璃珠,从滴定管中加入比预测定时少1毫升的样液,加热使其在2分钟内沸腾,趁热以先快后满的速度滴入样液,滴定时必须始终保持沸腾。待溶液颜色变浅时,以每2秒1滴的速度继续加入,直至蓝色刚好褪去即为终点,记录所消耗的葡萄糖标准溶液,平行做三次,取其平均值,计算结果:
X=A×100×250/(m×V×1000)
其中X代表还原糖含量,g/100g.
m代表样品质量,g。
V代表滴定时所消耗的葡萄糖标准溶液的体积,mL。
A代表10毫升碱性酒石酸铜溶液相当于葡萄糖的质量,mg。
250代表样液的总体积,mL。
五:数据处理:
项目六:香肠中亚硝酸盐的测定—盐酸萘乙二胺
一、目的要求
1.熟练掌握样品制备、提取的基本操作技能。
2.进一步学习并熟练掌握分光光度计的使用方法和技能。
3.学习N-1-萘乙二胺比色法测定亚硝酸盐的原理及操作要点。
二、实验原理
样品经沉淀蛋白质,除去脂肪后,在弱酸条件下,亚硝酸盐与对氨基苯磺酸重氮化后,在与盐酸萘乙二胺偶合形成紫红色染料,在538nm波长处有最大吸收,测定吸光度以定量(或与标准比较定量)。国标食品中亚硝酸盐含量不高于30mg?kg。
三、实验试剂与仪器
(1)、试剂
1、亚铁氰化钾溶液:称取10.6g亚铁氰化钾,用水溶解,并稀释至100ml.
2、乙酸锌溶液:称取22.0g乙酸锌,加3ml冰乙酸溶于水,并稀释至100ml.
3、饱和硼砂溶液:称取5.0g硼酸钠,溶于100ml热水中,冷却后备用.
4、对氨基苯磺酸溶液:4g/l,称取0.4g对氨基苯磺酸,溶于100ml20%盐酸中,置于棕色试剂瓶中混匀,避光保存.
5、盐酸萘乙二胺溶液:2g/l,称取0.2g盐酸萘乙二胺,溶于100ml水中,混匀后,置于棕色试剂瓶中,避光保存.
6、亚硝酸钠标准溶液:准确称取0.1000g与硅胶干燥器中干燥24h的亚硝酸钠,加水溶解入500ml容量瓶中,加水稀至刻度,混匀。此溶液相当于200ug的亚硝酸钠.
7、亚硝酸钠标准使用液:临用前,吸取亚硝酸钠标准溶液5.0ml置于200ml容量瓶中,加水稀至刻度,混匀。此溶液相当于5.0ug的亚硝酸钠.
(2)仪器、
分光光度计;小型绞碎机
四、实验步骤:
1.样品处理:
称取5.0g经绞碎混匀的香肠试样,置于50ml烧杯中,加12.5ml饱和硼砂溶液,搅拌均匀,以70℃左右的水约300ml将试样洗入500ml容量瓶中,与沸水浴中加热15min取出后冷却至室温,然后一面转动,一面加入5ml亚铁氰化钾溶液,摇匀,再加入5ml乙酸锌溶液,以沉淀蛋白质。加水至刻度,摇匀,放置0.5h,除去上层脂肪,清夜用滤纸过滤,弃去初滤液30ml,滤液备用。
2.测定:
吸取40ml上述滤液与50ml?∪?壬?苤校?砦??.00ml,0.20ml,0.40ml,0.60ml,0.80ml,1.00ml,1.50ml,2.00ml,2.50ml亚硝酸钠标准使用液(相当于0ug,1ug,2ug,3ug,4ug,5ug,7.5ug,10ug,12.5ug亚硝酸钠),分别置于50ml带塞比色管中。与标准管与试样管中分别加入2ml对氨基苯磺酸(4g/l),混匀,静置3—5min后各加入1ml盐酸萘乙二胺溶液(2g/l),加水至刻度,混匀,静置15min。用2cm比色杯,以零管调节零点,在波长538nm处测吸光度,绘制标准曲线比较,同时做试剂空白。
五、结果处理
1. 绘制标准曲线

2.结果计算
Ⅹ?m1×1000÷[m×?V2/V1?×1000]
= 0.8913×1000÷[5.0×?40/500?×1000]
=2.2283mg/kg
其中Ⅹ为样品中亚硝酸盐的含量;m为样品质量5g;m1为测定样液中亚硝酸盐的质量m1=0.082/0.092=0.8913(0.082为样品吸光度值);V1为样品处理液总体积500ml;V2为测定用样液体积40ml。
项目七:乳粉中蛋白质含量的测定
一、实验原理:
将样品与浓硫酸和催化剂一同加热消化,使蛋白质分离,其中碳和氢被氧化为二氧化碳和水逸出,而样品中的有机氮转化为氨,再与硫酸结合形成硫酸铵,此过程叫做消化。加入碱液,使氨游离出来,在通过水蒸气蒸馏,使氨流出,用硼酸吸收形成硼酸铵溶液,再用盐酸标准溶液滴定,根据消耗的盐酸标准溶液的体积即可算出蛋白质的含量。
二、实验试剂:
40%氢氧化钠溶液,0.1当量的盐酸溶液,浓硫酸,2%硼酸溶液,硒粉,消化管,定氮仪,消化电炉,电子天平,移液管,量筒。
三、实验步骤:
1、干燥:将清洗后的消化管放入干燥箱中干燥至内外比均无水珠即可。
2、消化:秤取2克乳粉和0.5克硒粉放入消化管中,加入10毫升浓硫酸,密封好放在消化炉中加热消化45分钟,放冷后备用。
3、蒸馏:向消化管中加入50毫升40%氢氧化钠溶液和10毫升水,放在定氮仪的长管下关口伸到页面下,固定好。清洗好一个锥形瓶加入50毫升2%硼酸溶液,再加入2到3滴指示剂,放在定氮仪的短管下,关口伸到页面下,接取蒸馏液至刻度在150毫升即可。
4、滴定:用0.1当量的盐酸标准溶液滴定蒸馏液至溶液颜色显淡紫色为止,记录下消耗的盐酸标准溶液。
5、空白滴定:清洗好一个锥形瓶加入50毫升2%硼酸溶液,再加入2到3滴指示剂,直接用0.1当量的盐酸标准溶液滴定蒸馏液至溶液颜色显淡紫色为止,记录下消耗的盐酸标准溶液。
四、数据处理:
X=C(V1-V2)×0.0140×F×100×100/(M×10)
其中: X代表蛋白质含量,g/100g,
C=0.1moL/L代表盐酸标准溶液的体积,
V1=2.1mL代表滴定时所消耗的盐酸标准溶液的体积,
V2=0.2mL代表滴定空白试验时所消耗的盐酸标准溶液的体积,
F=100/16代表氮换算成蛋白质时的系数,
M=2g代表称取的样品重。
五、结果计算:
将各数据带入式子算出结果为8.3125g/100g.
项目八:香肠中脂肪含量的测定-索氏抽提法
一:实验原理
将已经过预处理而干燥分散的样品,用无水乙醚进行提取,使样品中的脂肪进入溶剂中,然后从抽提液中回收溶剂无水乙醚,剩余的残留物即为脂肪或者粗脂肪,因为残留物中除了含游离脂肪外,还有磷脂、色素、树脂、蜡状物、挥发油、糖脂等,因此他测定的使粗脂肪,另外只有游离的脂肪才能用次方法测定。
二:实验仪器及试剂:
索氏抽提瓶,脂肪粗侧仪,滤纸,脱脂棉,无水乙醚。
三:实验步骤:
1、准备工作:将抽提瓶清洗干净放入105℃的干燥箱中除去水分,找一只比抽提瓶直径稍小的木棒,将滤纸缠绕在上面做成一个滤纸筒,用绳扎好,并在筒底部放入适量脱脂棉备用,同时在测定仪的水浴锅内加入适量水,并将水温调至78℃,预热。
2、样品处理:取适量样品与研钵中捣碎,然后随研钵一起放入105℃的干燥箱中干燥30分钟出去水分。
3、加药抽提:称取2克干燥后的样品放入滤纸筒中,加入50毫升无水乙醚
于滤纸筒内,并在脂肪粗侧仪固定好,打开开关,设定好抽提的时间和水的温度。
4、抽提液处理及无水乙醚的回收:抽提完后,经抽提瓶放入干燥箱中,使脂肪中的污水乙醚挥发殆尽,剩余的即为纯净的脂肪,同时将冷凝管中回收的乙醚重新倒回到棕色瓶中再次利用。
四:数据处理:
X=(A1-A2)×100/A3
其中X代表脂肪含量,g/100g,
A1代表干燥后抽提瓶和脂肪的总重,g,
A2代表干燥后抽提瓶的质量,g,
A3代表称取的样品的重量,g。
第一组:A1=115.222g A2= 114.96g A3=2.00g 带入算出X=13.1g/100g,
第二组:A1=111.552g A2= 111.32g A3=2.00g 带入算出X=11.6g/100g,
取平均值: X=12.35g/100g。
五:注意事项:
实验中所需的药品挥发性极高,对人体危害极大,因此加入药品时一定要小心,切记键入口、鼻、耳,尤其是眼睛中。
六:实验感受:
这个实验操作并不复杂,主要是仪器的操作使用,只不过是等待的时间太久而已,因此操作此实验一定要有耐心。
项目九:茶叶中氟的测定—氟离子选择电极法
一、 目的要求
1.理解选择电极法测定氟离子的基本原理。
2.掌握选择电极法测定氟离子的方法及操作要点。
二、实验原理
氟离子选择电极的氟化镧单晶膜对氟离子产生选择性的对数效应,氟电极和甘汞电极在被测试液中,电位差可随溶液中氟离子的活度的变化而变化,电位变化规律符合能斯特方程式。
氟电极和甘汞电极在溶液中组成一对电化学电池。利用电动势与离子活度的线性关系可直接求出样品溶液中的氟离子的浓度。
三、实验仪器
① 总离子强度调节缓冲液
a. 称取40.8g乙酸钠,溶于60ml水中,加1mol?L乙酸调节pH至7.0,加水稀释至100ml,此为3mol?L乙酸钠溶液。
b. 称取22g柠檬酸钠溶于60ml水中,加2.8ml高氯酸,在加水稀释至100ml,此为0.75mol?L柠檬酸钠溶液。
c. 取3mol?L乙酸钠溶液与0.75mol?L柠檬酸钠溶液等量混合,即为总离子强度调节缓冲液。临用时配制。
② 氟标准溶液:1ug氟?ml。
四、测定步骤
称取2.00g的样品,置于100ml容量瓶中,加20mol?L盐酸,密闭浸泡提取提取1h(不是轻轻摇动),应尽量避免样品粘于瓶壁上,提取后加50ml总离子强度调节缓冲液,加水至刻度,混匀备用。
吸取0.0ml、1.0ml、2.0ml、5.0ml、10.0ml氟标准使用液(相当0ug、1ug、2ug、
5ug、10ug氟),分别置于50ml容量瓶中,于各容量瓶中加入25ml总离子强度调节缓冲液、10ml盐酸,加水至刻度,混匀备用。
将氟和甘汞电极与测量仪器的负端和正端相连接。电极插入盛有水的25ml塑料杯中,在电磁搅拌下读取平衡电位值,更换2~3水,待电位值平衡后,即可进行样液和氟标准使用液的电位测定。
以电极电位为纵坐标、氟离子浓度为横坐标,在半对数坐标纸上绘制的标准曲线为:

五、结果计算
X=AV×1000/m×1000
=5.9 ×100×1000/2×1000
=295mg/kg
X为样品中氟的含量mg/kg;A为测定样品氟的浓度5.9ug/ml;m为样品质量2g;V样液总体积100ml。

