桔皮中果胶提取技术的试验分析
【摘要】酸浸提法提取果胶具有快速、简便、易于控制、提取率较高等特点,用盐酸浸提、乙醇沉淀法进行了从桔皮中提取果胶的工艺试验。用单因素试验进行工艺参数的优化,其适合的工艺条件是:液料质量比为20;浸提液pH值为2;浸提温度为90℃。
关键词:桔皮 果胶 提取工艺 工艺参
引言:果胶是一种亲水性植物胶,属于多糖类物质,广泛存在于高等植物的根、茎、叶、果的细胞壁中。通常人们所说的果胶系指原果胶、果胶和果胶酸的总称,是一种高分子聚合物,分子量介于20 000-400 000之间。其基本结构是D一吡喃半乳糖醛酸,以1,4甙链连接成的长链,其中部分半乳糖醛酸被甲醇酯化[1]。
胶凝剂、增稠剂、稳定剂和乳化剂,随着功能性多糖的开发研究,果胶作为水溶性膳食纤维,越来越受到重视。应用必定会越来越广泛[2-4]。我国是柑桔的主要产地,柑桔皮中果胶含量可达10% ~30%。从桔皮中提取果胶不仅有极大的工业价值,而且对综合开发、利用柑桔资源,提高原材料利用率,减少环境污染,有重要的实际意义[2,4,6]。果胶的提取一般有酸提取法、离子交换法、微生物法和微波加热处理法等方法[5-9],由于酸提取法具有快速、简便且提取率高的优点,国内外大多采用此法。果胶分离沉淀主要有乙醇沉淀法和盐析法。国内主要采用乙醇沉淀法,而国外多用盐析法或不经沉淀直接喷雾干燥。针对我国情况而言,对乙醇沉淀法已有大量研究,而本实验也是在总结别人成果的基础上进行对比以及提取工艺条件的优化。
1材料与方法
1.1 材料
桔皮采用成熟新鲜、无病虫果害的晚熟蜜桔,人工取皮,在40℃下干燥,粉碎至1~3 mm,待用。
盐酸、乙醇、氢氧化钠、无水氯化钙、冰醋酸和甲基红,均为化学纯。
1.2 果胶提取方法
果胶提取工艺为:原料→洗涤→失活→干燥→粉碎→酸提取→过滤→浓缩→冷却→乙醇沉淀→离心分离→干燥→称量→粉碎→果胶。
剔除腐烂变质、发黑的桔皮,用清水洗净后,放入烧杯中,加水,加热至90 ℃保温5~10 min,使酶失活,捞出桔皮,将桔皮在40 ℃下干燥,切碎。将20 g原料加入用HC1预先配制的、具有一定pH值和温度的酸溶液中,维持所需的温度达到一定的提取时间,并不断搅拌。趁热用布氏漏斗过滤得果胶提取液。将滤液用旋转蒸发仪在60-70 ℃下浓缩至原体积的1/3时为止。果胶浸提液冷却至常温后加入1倍体积的95 乙醇,搅拌、静置2 h,使果胶沉淀析出。用布氏漏斗过滤得粗果胶。在60-70 ℃干燥,粉碎即得果胶粉。随后进行提取物中果胶含量的测定和提取率的计算。
1.3 试验方法
单因素试验,分别研究不同液料质量比对果胶提取率的影响(浸提液pH值3、温度80℃、浸提时间45 min);不同浸提液pH值对果胶提取率的影响(浸提液温度80℃、液料质量比10、浸提时间45 min);不同浸提液温度对果胶提取率的影响(液料质量比10、浸提液pH值3、浸提时间45 min)。
1.4果胶提取率
果胶提取率表示为
DP=B/E*100%
式中B一提取的果胶量,E——原料量(g)。
1.5 仪器设备
恒温水浴锅、旋转蒸发仪、电热干燥箱、可用精密pH试纸、电子天平、布氏漏斗、抽滤瓶、玻棒、尼龙布、表面皿、烧杯、小刀、真空泵。
2结果与分析
2.1 液料质量比对果胶提取率的影响
液料质量比对提取率影响如图1所示。液料质量比太小,则难以保证原料中的果胶质全部转移到液相中,物料粘度大、过滤困难、残留增多 造成提取不完全、提取率低;液料质量比太大,提取出来的果胶质在溶液中的含量太低,过滤容易,但是浓缩所需的时间长、沉淀剂乙醇的消耗量大,沉淀效果不理想。因此,提取果胶所用酸液量的多少,直接影响到已水解的可溶性果胶能否全部转移至液相,同时也影响提取液过滤速度,以及蒸发浓缩时的能耗。

图1 液料比与果胶提取率的关系曲线
Fig.1 Relationship between solution/material ratio and
extract rate of pection
从图1中可以看出,当提取的液料质量比大于20时,果胶提取率随液料质量比的增大而减小;当提取的液料质量比小于20时,果胶提取率随液料质量比的减少而减小;当提取的液料质量在20时,提取效果较好。
2.2 提取液pH值对果胶提取率的影响
提取液pH值对提取率的影响如图2所示。提取液pH值小,则酸度太强,果胶在提取过程中水解过度,致使果胶脱去酯基和裂解而使提取率下降,同 时使产品色泽变深而不合要求;而pH值大时,果胶提取率有降低趋势。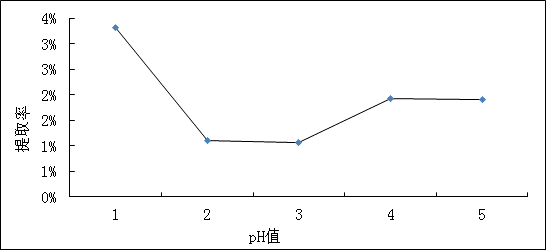
图2 提取液pH值和果胶提取率的关系曲线
Fig.2 Relationship between pH of extract solution
and extract rate of pection
从图2中可以看出,提取液pH值为2时,果胶的提取率较高;当pH值大于2时,随着pH值的增大,果胶提取率降低;当pH值大于4时,随着pH值的增大,果胶提取率缓慢上升最后趋于水平,得出结论一定范围内pH对提取不利。
2.3 提取沮度对果胶提取率的影响
提取温度对提取率影响如图3所示。随着提取温度的升高,有利于果胶质的水化溶出,有利于提取效率的提高。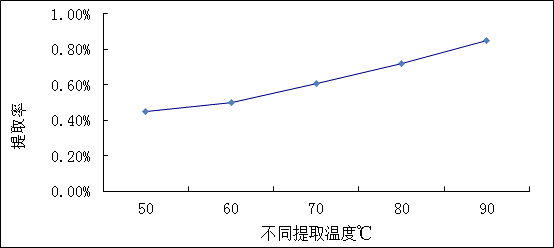
图3 提取温度和果胶提取率的关系曲线
Fig.3 Relationship between temperature and
extract rate of pectin
从图3中可以看出,在90℃左右时,提取率最高;整个过程,随着温度的升高,提取率逐步提高。
3讨论
从上面的数据可以看出每组的果胶绝对数值都很少,原因之一是我们的操作是切碎后煮的,那么煮的时候使其中的果胶流失严重,虽然不会影响到对整个趋势的研究,但因为绝对数量的减少,使趋势对操作误差十分敏感,从而使规律出现偏差。在用乙醇沉淀时,要求快速冷却,这个条件做的程度不够,且每组也有差异。还有就是因为沉淀出来的果胶是絮状物,在过滤的时候,第一是过滤效果不好,其次是一部分果胶被滤到了滤液中使提取率偏低。
由于柑桔产地不同、品种好不同、成熟度不同,其果皮的果胶含量也会不尽相同,因此,用酸提取果胶所采用的条件也稍有差异。生产过程采用以干质原料提取果胶会更为实际,且将干燥后的桔皮切碎,可增大接触面积、缩短提取时间、提取较完全,从而增加产量。水中的钙、镁离子对原果胶有一定的封闭作用,使其难于转化成水溶性果胶,所以水的软化处理对果胶的提取十分重要 引。桔皮中本身所含的钙、镁离子及其它杂质,也会影响果胶的溶解和纯度[10-11],用醇沉淀果胶时必须快速冷却滤液,这样可减少果胶脱脂而使其受破坏,又可以减少沉淀剂的用量。应尽量缩短加酸提取到乙醇沉淀之间的时间,因为酸对果胶分子的酯键具有破坏作用,随着作用时间的延长,其破坏性增大,结果会使果胶分子量逐渐变小,导致果胶的胶凝度下降,质量变差。根据果胶用途,决定是否脱色。如用果胶制取有色产品,则需保留原来的桔黄色;若要脱色,可用活性炭、活性白土、膨胀珍珠岩等作为脱色剂进行脱色处理[11]。
4结论
通过盐酸浸提法从桔皮中提取果胶的单因素试验研究表明,当浸提的pH值为2,温度为90℃左右,液料质量比为20时,果胶提取效果最好。
参考文献
1 田三德,任红涛.果胶生产技术工艺现状及发展前景.食品科技,2003(1):53-55
2 王金英,马中国,宗灿华.果胶的提取与应用.中国林副特产,2000,53(2):17~18
3 尹湘廷,李玉环,陈恭正.以桔皮为原料提取果胶的研究.信阳师范学院学报,1994,7(3):295~296
4 李于善,张争光,李啸等.果胶的提取研究.三峡大学学报,2002,24(6):571~573
5 黄希俊.桔皮的综合利用.应用科技,1998,25(9):9
6 马福波.从桔皮中提取柑桔黄、桔油、果胶的技术研究.贵州化工,1996,21(3):40~43
7 张鸿发,励建荣,周勤等.从柑桔皮中连续提取色素、果胶的工艺研究.食品科学,2000,21(1I):37~38
8 田旭东,贾怀锋.由柑桔皮生产果胶.化学教育,2000,21(12):28
9 侯春友,刘钟栋,陈肇锬.微波条件下提取果胶的研究.郑州粮食学院学报,1999,20(2):8~12
10 叶忠,项有剑,钱伦波.从桔皮中提取果胶条件的探讨.温州师范学院学报,1995(3).67~68
11 肖红,吴永娴,曾凡坤.橙皮果胶制备中提取和除杂的研究.海南大学学报自然科学版,2000,18(1);33~39
第二篇:果胶的提取实验报告
综合设计性实验报告
实验题目:柑橘皮中果胶的提取及其在果酱制备中的应用
学 院:
姓 名:
学 号:
班 级:
20xx-12-2
果胶广泛存在与水果和蔬菜中,如苹果含量为0.7~1.5%(以湿品计),在蔬菜中以南瓜含量最多,为7~17%。果胶的基本结构是以α-1,4-糖苷键连接的聚半乳糖醛酸,其中部分羧基被甲酯化,其余的羧基与钾、钠、钙离子结合成盐。
在果蔬中,尤其是未成熟的水果和皮中,果胶多数以原果胶存在,原果胶是以金属离子桥(特别是钙离子)与多聚半乳糖醛酸中的游离羧基相结合。原果胶不溶于水,故用酸水解,生成可溶性的果胶,再进行脱色、沉淀、干燥,即为商品果胶,从柑橘皮中提取的果胶是高酯化度的果胶,酯化度在70%以上。在食品工业中常利用果胶来制作果酱、果冻和糖果,在汁液类食品中用作增稠剂、乳化剂等。
一、实验的目的及原理
1.1 实验目的
⑴ 掌握果胶提取的方法;
⑵ 掌握果胶的形成凝胶的条件和成胶机理;
(3)探求果胶在果酱制备中的应用。
1.2 实验原理
原料经酸处理后,加热至90℃,将不溶性的果胶转化为可溶性果胶,然后乙醇处理提取液,使果胶沉淀,再用乙醇洗涤沉淀,以除去可溶性糖类、脂肪、色素等物质,得到较为纯净的果胶物质。
二、实验方案设计
2.1 实验材料与设备
桔皮(新鲜)
0.25%HCl、95%乙醇、蔗糖、柠檬酸
250ml烧杯*2、电炉、温度计、小刀、纱布、0.25%的盐酸60ml、ph试纸、漏斗、0.5~1.0%的活性炭、抽滤装置(或2~4%的硅藻土)、稀氨水、95%乙醇、柠檬酸0.1g、柠檬酸钠0.1g和蔗糖20g
2.2 实验方案设计
果胶的提取
⑴ 原料预处理
称取新鲜柑橘皮20g(干品为8g)用清水洗净后,放入250ml烧杯中加120ml水,加热至90℃保持5~10min,使酶失活。用水冲洗后切成3~5mm大小的颗粒,用50℃左右的热水漂洗,直至水为无色、果皮无异味为止。每次漂洗必须把果皮用纱布挤干,再进行下一次漂洗。
⑵ 酸水解提取
将预处理过的果皮粒放入烧杯中,加入约0.25%的盐酸60ml,以浸没果皮为度,pH调整在2.0~2.5之间,加热至90℃并恒温45min,趁热用四层纱布过滤。
⑶ 脱色
在滤液中加入0.5~1.0%的活性炭于80℃加热20min进行脱色和除异味,趁热抽滤,如抽滤困难可加入2~4%的硅藻土作助滤剂。如果柑橘皮漂洗干净,提取液为清澈透明,则不用脱色。
⑷ 沉淀
待提取液冷却后,用稀氨水调节至pH3~4,在不断搅拌下加入95%乙醇,加入乙醇的量约为原体积的1.3倍,使酒精浓度达50~60%(加1/3酒精),静置10min。
⑸ 过滤、洗涤、烘干
用纱布过滤,果胶用95%乙醇洗涤二次,再在60~70℃下烘干。
柠檬味果酱的制取
⑴ 将果胶0.2g(干品)浸泡于20ml水中,软化后在搅拌下慢慢加热至果胶全部溶化。
⑵ 加入柠檬酸0.1g、柠檬酸钠0.1g和蔗糖20g,在搅拌下加热至沸,继续熬煮5min,冷却后即成果酱。
参考文献:《基础化学实验》上册,徐家宁,门瑞芝,张寒琦主编,高等教育出版社,2006。

