北京市西城区高中化学必修1第一章从实验学化学检测题B卷
一、选择题(每小题只有1个选项符合题意)
1. 实验室盛装浓硫酸的试剂瓶应贴有的安全使用标识是 ( )



2. 实验中的下列操作正确的是 ( )
A. 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B. Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道
C. 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D. 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
3. 实验操作均要用玻璃棒,其中玻璃棒作用相同的是 ( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A. ①和② B. ①和③ C. ③和④ D. ①和④
4. 下列分离和提纯的实验,所选用的方法和仪器不正确的是 ( )
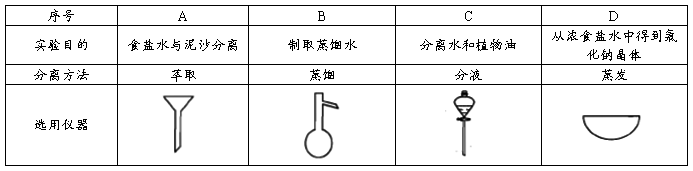
5. 下列实验操作或结论正确的是 ( )
A. 分液时,先将上层液体倒出
B. 将烧杯中刚溶解的氢氧化钠溶液立即转移到容量瓶中
C. 粗盐经溶解、过滤、蒸发结晶得到的食盐中,仍含有Mg2+、Ca2+、SO 等杂质
等杂质
D. 制取蒸馏水时,冷却水应由冷凝器的上口通入,下口流出
6. 下列叙述正确的是 ( )
A. 1 mol H2O的质量为18g/mol
B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子的质量为32g
D. 标准状况下,1 mol任何物质体积均为22.4L
7. 已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是 ( )
A. 16g B. 32g C. 64g/mol D. 32g/mol
8. 科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是 ( )
A. 原子数 B. 分子数 C. 体积 D. 物质的量
9. 同温同压下,等质量的下列气体所占有的体积最大的是 ( )
A. O2B. CH4C. CO2D. SO2
10. 0. 5 L 1 mol/L FeCl3溶液与0.2 L lmol/L KCl溶液中的Cl-的数目之比 ( )
A. 5:2 B. 3:1 C. 15:2 D. 1:3
11. 为了除去粗盐中Ca2+、Mg2+、SO 及泥沙,将粗盐溶于水,然后进行下列操作:
及泥沙,将粗盐溶于水,然后进行下列操作:
①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液
⑤加过量的BaCl2溶液,正确操作的顺序是 ( )
A. ②⑤④①③ B. ④①②⑤③
C. ①④⑤②③ D. ⑤②③④①
12. 下列说法中,正确的是 ( )
A. 22. 4 L N2含阿伏加德罗常数个氮分子
B. 在标准状况下,22. 4 L 水的质量约为18g
C. 22g二氧化碳与标准状况下11.2 L HCI含有相同的分子数
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
13. 实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是 ( )
A. 950 mL 111. 2 g B. 1000 mL 11 7 g
C. 500 mL 117 g D. 任意规格111.2 g
14. 设NA为阿伏加德罗常数,下列说法中,正确的是 ( )
A. 2. 4 g金属镁所含电子数目为0.2 NA
B. 1 mol H2SO4所含粒子数目为NA
C. 1 7 g NH3所含中子数目为10 NA
D. 18 g水所含分子数目为NA
15. 现有三组溶液:①汽油和氯化钠溶液;②39%的乙醇水溶液;③氯化钠和单质溴的水溶液。分离以上各混合液的正确方法依次是 ( )
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
16. 用NaOH固体配制1 mol/L的NaOH溶液,下列操作和说法中正确的是 ( )
A. 将40 g NaOH固体溶于1L水中可配成1 mol/L的NaOH溶液
B. 称量时,将固体NaOH直接放在天平右盘上
C. 固体溶解后冷却到室温,然后将溶解后溶液转移到容量瓶中,立即向容量瓶中直接加水稀释到刻度线
D. 配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
17. 下列各组物质中,所含分子数相同的是 ( )
A. 1gH2和lgO2B. 5. 6 LN2(标准状况)和22gCO2
C. 9gH2O和0.5 molCl2D. 22.4 LH2(标准状况)和0. 1 mol N2
18. 设NA阿伏加德罗常数,下列说法正确的是 ( )
A. 5.6g金属铁与足量稀盐酸充分反应,失去的电子数为0.3NA
B. 常温常压下,9 g H2O中含有的分子数为NA
C. 标准状况下,11.2 LSO2中含有的氧原子数为NA
D. 1g12C中所含有的碳原子数为NA
19. 取物质的量浓度为0.05 mol/L的金属氯化物(RClx)溶液20 mL,使之恰好与20 mL0.15 mol/L的AgNO3溶液完全反应。则该氯化物的化学式为 ( )
A. RCl B. RCl2C. RCl3D. RCl4
20. 甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸4种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙十丁→沉淀;乙+丁→无色无味气体。则甲、乙、丙、丁4种溶液依次是 ( )
A. BaCl2、Na2CO3、盐酸、AgNO3B. BaCl2、Na2CO3、AgNO3、盐酸
C. Na2CO3、盐酸、AgNO3、BaCl2D. AgNO3、盐酸、BaCl2、Na2CO3
二、填空题
21. 现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。
若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为mol。
(2)该气体所含原子总数为个。
(3)该气体在标准状况下的体积为L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为。
(5)该气体溶于水后形成VL溶液. 其溶液的物质的量浓度为mol/L。
22. 草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾。现从草木灰中提取钾盐,并用实验检验其中的CO 、SO
、SO 和Cl?。
和Cl?。
(1)从草木灰中提取钾盐的实验操作顺序如下:①称取样品,②溶解沉降,③,④蒸发结晶。
(2)在进行②③④操作时,都要用到玻璃棒,其作用分别是:
②。
③。
④。
(3)将制得的少量晶体放入试管,加热蒸馏水溶解并把溶液分成三份,分装在3支试管里。
① 在第一支试管里加入稀盐酸,可观察有生成,证明溶液中有离子。
② 在第二支试管里加入足量稀盐酸后,再加入BaCl2溶液,可观察到有______生成,证明溶液中有离子。
③ 在第三支试管里加入足量稀硝酸后,再加入AgNO3溶液,可观察到有生成,证明溶液中有离子。
三、简答题
23. 甲、乙两人分别用不同的方法配制100 mL 3.6 mol/L的稀硫酸。
(1)甲:量取20 mL 18 mol/L浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
① 实验所用的玻璃仪器除烧杯和容量瓶外,还有;
② 将溶液转移到容量瓶中的正确操作是
;
③ 定容的正确操作是。
(2)乙:用100 mL量筒量取20 mL浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处。
24. 下图的实验装置用来分离CO2和CO气体并干燥。图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽。为使实验成功,甲、乙、丙分别盛放的溶液是(填字母),原因是
。
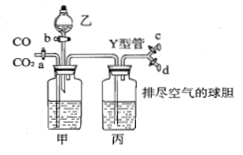
A. NaHCO3饱和溶液、12 mol/L盐酸、18. 4 mol/L H2SO4
B. Na2CO3饱和溶液、2 mol/L H2SO4、NaOH饱和溶液
C. NaOH饱和溶液、2 mol/L H2SO418.4 mol/L H2SO4
D. 18. 4 mol/L H2SO4、NaOH饱和溶液、18. 4 mol/L H2SO4
四、计算题
25. 常温下,在27. 5 g水中溶解12. 5 g CuSO4·5H2O,恰好达到饱和,该溶液密度为1. 21 g/cm3,求:
(1)该溶液中阴阳离子的总物质的量。
(2)该溶液中CuSO4的物质的量浓度。
(3)取出20. 0 mL该溶液,配成浓度为1. 00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
【试题答案】
一、选择题
1. A 2. D 3. D 4. A 5. C 6. C 7. D 8. A 9. B 10. C
11. A 12. C 13. B 14. D 15. C 16. D 17. C 18. C 19. C 20. B
二、填空题
21. (1)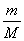 (2)
(2)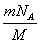 (3)
(3)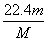 (4)
(4)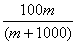 %
%
(5)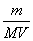
22. (1)过滤
(2) ② 搅拌,促进固体溶解
③ 引流,防止液体流到滤纸外 。
④ 搅拌,防止液体局部过热,发生暴沸
(3) ① 无色气体CO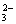 ② 白色沉淀SO
② 白色沉淀SO ③ 白色沉淀Cl?
③ 白色沉淀Cl?
三、简答题
23. (1)①量筒、玻璃棒、胶头滴管②将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地倒入容量瓶中 ③加水至离刻度线1~2cm时,改用胶头滴管滴加水至液面与刻度线相切
(2)不能用量筒配制溶液,不能将水加入到浓硫酸中
24. C 甲中试剂用于吸收CO2排除A、D两选项;乙中试剂用于“还原”回CO2;丙中试剂用于干燥两种气体,排除B选项。
四、计算题
25. (1)0. 100 mol (2)1.51 mol/L (3)30. 2 mL
第二篇:成才之路20xx-20xx高一化学人教版必修1达标作业:第1章+第2节+第3课时《物质的量在化学实验中的应用》
第一章第二节第3课时

一、选择题
1.(2013·嘉积中学高一期末)下列溶液中,Na+的物质的量浓度最大的是( )
A.1 mL 0.5 mol·L-1的NaOH溶液
B.100 mL 0.01 mol·L-1的NaCl溶液
C.100 mL 0.1 mol-1的NaOH溶液
D.10 mL 0.1 mol·L-1的Na2SO4溶液
【解析】 A项c(Na+)=0.5 mol·L-1;B项,c(Na+)=0.01 mol·L-1;C项,c(Na+)=0.1 mol·L-1;D项,c(Na+)=0.2 mol·L-1。
【答案】 A
2.(2013·箴言中学高一月考)下列溶液中的Cl-浓度与50 mL 1 mol·L-1MgCl2溶液中的Cl-浓度相等的是( )
A.150 mL 1 mol·L-1NaCl溶液
B.75 mL 2 mol·L-1CaCl2溶液
C.150 mL 2 mol·L-1KCl溶液
D.75 mL 1 mol·L-1AlCl3溶液
【解析】 50 mL 1 mol·L-1MgCl2溶液中c(Cl-)=2 mol·L-1,A项,c(Cl-)=1 mol·L-1;B项,c(Cl-)=4 mol·L-1;C项,c(Cl-)=2 mol·L-1;D项,c(Cl-)=3 mol·L-1。
【答案】 C
3.(2013·福州八中高一检测)将4 g NaOH溶解于水配成1 L溶液,从中取出10 mL,这10 mL溶液的物质的量浓度是( )
A.1 mol/L B.0.1 mol/L
C.0.01 mol/L D.10 mol/L
【解析】 c===0.1 mol·L-1。
【答案】 B
4.(2013·威武市六中高一检测)在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1 mol/L,加入等体积0.3 mol/L的BaCl2溶液恰好使SO完全沉淀,则混合溶液中Na+的浓度为( )
A.0.3 mol/L B.0.45 mol/L
C.0.6 mol/L D.0.15 mol/L
【解析】 设混合液体积为1 L。n(Al3+)=c·V=0.1 mol/L×1 L=0.1 mol,n(SO)=n(Ba2+)=0.3 mol/L×1 L=0.3 mol。由电荷守恒可得:3n(Al3+)+n(Na+)=2n(SO),所以n(Na+)=2n(SO)-3n(Al3+)=2×0.3 mol-3×0.1 mol=0.3 mol,c(Na+)====0.3 mol/L。
【答案】 A
5.(2013·箴言中学高一月考)实验室里需用480 mL 0.1 mol/L的硫酸铜溶液,现选取500 mL容量瓶进行配制,以下操作正确的是(说明:胆矾为五水硫酸铜)( )
A.称取7.68 g硫酸铜,加入500 mL水
B.称取12.0 g胆矾,配成500 mL溶液
C.称取8.0 g硫酸铜,加入500 mL水
D.称取12.5 g胆矾,配成500 mL溶液
【解析】 胆矾化学式为CuSO4·5H2O,摩尔质量为250 g·mol-1。配制500 mL 0.1 mol/L CuSO4溶液,需胆矾的物质的量为:n(CuSO4·5H2O)=c·V=0.1 mol·L-1×0.5 L=0.05 mol,其质量为m(CuSO4·5H2O)=n·M=0.05 mol×250 g·mol-1=12.5 g,将12.5 g胆矾溶于水配成500 mL溶液。
【答案】 D
6.(2013·惠阳中学高一检测)现有VL 0.5 mol/L的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是( )
A.加热浓缩到原来体积的一半
B.加入0.05 mol/L的盐酸0.125VL
C.加入10 mol/L的盐酸0.1VL,再稀释至1.5VL
D.标况下通入11.2 L氯化氢气体
【解析】 A项加热时盐酸先挥发出HCl,A项错;
B项:c混==0.5 mol/L,B项错误;
C项:c混==1 mol/L,C项正确;
D项:c混== mol/L,D项错误。
【答案】 C
7.(2013·福州八中高一检测)配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已吸潮
B.向容量瓶中加水时液面低于刻度线即摇匀
C.有少量NaOH溶液残留在烧杯内
D.没有洗涤烧杯和玻璃棒
【解析】 根据c==进行判断。NaOH已潮湿,称量的NaOH的质量小,浓度偏低,A项错误;向容量瓶中加水时液面低于刻度线,加水加得少了,所以浓度偏高,B项正确;有少量NaOH溶液残留在烧杯内,使n变小,浓度偏低,C项错误;未进行洗涤,使n减小,故使浓度偏低,D项错误。
【答案】 B
8.(2014·试题调研)已知某饱和氯化钠溶液的体积为VmL,密度为ρg·mL-1,质量分数为w,物质的量浓度为cmol·L-1,溶液中所含NaCl的质量为mg。下列选项正确的是( )
A.该温度下NaCl的溶解度S= g
B.溶液中溶质的物质的量浓度c(NaCl)= mol·L-1
C.溶液中溶质的物质的量浓度c(NaCl)= mol·L-1
D.溶液中溶质的质量分数w=%
【解析】 选项A,100 g?S=(1-w)?w,即S= g。选项B,c(NaCl)== mol·L-1。选项C,c(NaCl)== (mol·L-1)。选项D,由c=,则w=×100%。
【答案】 C
【点拨】 溶液的物质的量浓度与溶质的质量分数之间的换算公式为c=,其中ρ为溶液的密度(g/cm3),w为溶质的质量分数,M为溶质的摩尔质量(g/mol),由上述公式可知,已知ρ、w、M,就可以求出c,用公式法计算时要特别注意单位之间的换算。
9.用NA代表阿伏加德罗常数,相关说法不正确的是( )
A.13.5 g Al与足量盐酸反应生成H2的分子数为NA
B.标准状况下,2.24 L CH4所含电子数为NA
C.500 mL 1 mol·L-1的K2SO4溶液中含有K+数目为NA
D.0.5 mol O2和0.5 mol O3的混合物所含有的氧原子个数为2.5NA
【解析】

【答案】 A
10.实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19 g·cm-3,则物质的量浓度是( )
A.11.9 B.11.9 mol·L-1
C.0.012 mol·L-1D.无法计算
【解析】 c(HCl)==11.9 mol/L。
【答案】 B
二、非选择题
11.(2013·南郑中学高一期中)
(1)质量都是50 g的HCl、NH3、CO2、O2四种气体中,含分子数最少的是________;同温同压下,密度最小的是________(填分子式)。
(2)标准状况下,33.6 L HCl气体溶于水配成1 L溶液,则溶液中溶质的物质的量浓度为________ mol/L。
(3)质量分数为49%的硫酸溶液,其密度为1.4 g/cm3,则其物质的量浓度为________mol/L。
(4)有一种气体的质量是14.2 g,在标准状况下的体积是4.48 L,则该气体的摩尔质量为________g/mol。
【答案】 (1)CO2 NH3 (2)1.5 (3)7 (4)71
12.实验室配制0.1 mol·L-1的BaCl2溶液可分两个阶段进行:第一阶段:用托盘天平称取5.2 g无水BaCl2晶体。第二阶段:溶解配制0.1 mol·L-1的BaCl2溶液。
第一阶段操作有如下几步:
A.将游码拨到0.2 g处;
B.将游码拨至“0”处;
C.在天平两边的托盘上各放一张干净的等质量的滤纸,调节天平两边的螺母使天平平衡;
D.取走药品,将砝码放回砝码盒内;
E.往左盘内逐步添加晶体至天平平衡;
F.在右盘上放置5 g砝码。
(1)其正确的操作顺序是(填序号):
B→( )→( )→A→( )→( )→( )
(2)在E操作中,只缺少量晶体时,其操作方法是________________________________
________________________________________________________________________。
(3)第二阶段操作,应先将5.2 g BaCl2加适量蒸馏水溶解,溶解过程中使用的主要仪器有________,然后将溶液转入________中,再经________、________、________后即可得到0.1 mol·L-1BaCl2溶液。
(4)下列操作使配制的BaCl2溶液浓度偏低的有________。
A.将砝码放在左盘上,BaCl2放在右盘上进行称量
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡
(5)100 mL容量瓶中盛有100 mL 0.1010 mol·L-1的BaCl2溶液,现欲将其稀释成浓度为0.100 mol·L-1的BaCl2溶液,所选用的仪器有:10 mL量筒、1 mL移液管(可准确移取0.1 mL~1.00 mL溶液)、酸式滴定管、胶头滴管。其简单的操作步骤是_______________________________。
【解析】 (1)使用托盘天平的步骤为:调零→放砝码→调游码→加物品→取物品→取砝码→游码回零。
(2)只缺少量晶体时,应用右手轻轻拍打左手手腕,小心振动药匙加足药量。
(3)溶解所需的仪器有烧杯、玻璃棒。
(4)误差分析根据c==,由m、V的大小判断。A将砝码放错位置后,称BaCl2为4.8 g,故偏低,B无影响,C摇匀后再加水即增大了溶液体积,故偏低。D不振荡,溶液不均匀。
(5)如果稀释较大倍数,可选用适宜的容量瓶稀释至相应的体积,但现在浓度改变较小,故只能吸取过多的溶质,然后再加水定容至刻度线。现过量的BaCl2仅为100 mL×10-3L/mL×(0.1010 mol·L-1-0.100 mol·L-1)÷0.1010 mol/L≈0.10 mL。
【答案】 (1)C F E D B
(2)左手拿药匙,用右手轻轻拍左手手腕,小心振动药匙加足药量,使天平平衡
(3)烧杯、玻璃棒 250 mL容量瓶 洗涤 定容 摇匀
(4)AC
(5)用1 mL移液管从容量瓶中移取0.10 mL BaCl2溶液,然后再用胶头滴管小心加蒸馏水至刻度线,盖好瓶塞,反复倒转摇匀即得0.100 mol·L-1的BaCl2溶液
13.(2014·试题调研)将117 g NaCl溶于水配制成1 L溶液,
(1)该溶液中NaCl的物质的量浓度为________,溶液中Cl-的物质的量浓度为________。
(2)配制1 mol·L-1的NaCl溶液500 mL,需该溶液的体积为________。
(3)向该溶液中再通入一定量的HCl气体后,溶液中Cl-的物质的量浓度为3 mol·L-1(假设溶液体积不变),则溶液中H+的物质的量浓度为________,通入HCl气体的体积(标准状况下)为________。
【解析】 (1)n(NaCl)==2 mol,
c(NaCl)===2 mol·L-1,
c(Cl-)=c(NaCl)=2 mol·L-1。
(2)配制500 mL 1 mol·L-1的NaCl溶液所需NaCl的物质的量为1 mol·L-1×0.5 L=0.5 mol,
设需要该溶液的体积为V,则有
0.5 mol=2 mol·L-1×V,V=0.25 L。
(3)根据溶液中电荷守恒定律
c(H+)+c(Na+)=c(Cl-)
c(H+)=c(Cl-)-c(Na+)=c(Cl-)-c(NaCl)
=3 mol·L-1-2 mol·L-1
=1 mol·L-1
溶液中n(H+)=1 mol·L-1×1 L=1 mol
n(HCl)=n(H+)=1 mol
V(HCl)=22.4 L·mol-1×1 mol=22.4 L。
【答案】 (1)2 mol·L-1 2 mol·L-1
(2)0.25 L
(3)1 mol·L-1 22.4 L
【特别提醒】 本题可以根据物质的量浓度的概念以及溶质的质量、物质的量和摩尔质量之间的关系进行计算,同时要熟练运用定组成规律和电荷守恒定律。

