溶解热的测定实验报告
一·实验目的
1.用简单量热计测定硝酸钾的溶解热
2·学习量热计热容的标定方法
3·非绝热因素对实验影响的校正
4·学会使用《计算机全程管理系统》
二·实验原理
无机盐类的溶解,同时进行晶格的破坏(吸热)和离子的溶剂化(放热)过程。将杜瓦瓶看作绝热体系,当盐溶于水中时,有如下热平衡:
ΔH(W/M)=KΔT1
式中,K为量热计热容
上述过程完成后,进行电标定,用点加热器加热,又有平衡:IVt=K ΔT2
左边是加热电功的计算
由此可得:
ΔH=(M/W)IVt(ΔT1/ΔT2)
由于在此两过程中,体系温度变化小,一般在1度左右,必须使用贝克曼温度计或精密电子温差仪,才能读到千分位,达到实验的要求。
也可以使用热敏电阻作为测温元件,它作为直流电桥的一个臂。热敏电阻因温度变化而电阻发生变化,电桥即有电阻输出。用自动平衡记录仪记录,或经放大后由计算机采集,用无纸记录仪记录。
由于温度变化小,可认为电桥输出与温度变化成正比。如果以上两过程为l1和l2,可用下式计算溶解热:
ΔH=(W/M)IVt(l1/ l2)
由于杜瓦瓶并非真正的绝热体系,实验过程中实际有微小的热交换。必须对温度进行校正。采用外推法,从时间-温度曲线上反映前后平均温度的点引时间坐标的垂线,与反应前后温度变化的延长线香蕉,交点的距离为l1和l2
三·仪器与试剂
500mL杜瓦瓶,装配有加热电炉丝和固体试样加料漏斗 克曼温度计或精密温差仪或测温热电阻(配有电桥)
电磁(或电动)搅拌仪 直流稳压电源(0~30V,0~2A)
直流电流表(0.5级,0~1.5A) 500mL量筒 停表
记录仪 分析纯硝酸钾
四·试验步骤
1·杜瓦瓶中用量筒加450mL水,装置好量热计,开始搅拌。调节输出为0,开启记录仪,记录体系温度稳定过程。
2·分析天平称取硝酸钾(前先碾成细粉,约3.3g),在量热计温度稳定3~5分钟后,从加料漏斗加入,记录仪记录过程温度变化。注意:加料漏斗加料前后应加盖,以减少体系与环境的热交换)
3·待温度没有明显变化后约3分钟停止记录。
4·电标定过程与上述过程类似操作,即分为标定前期、标定期和标定后期。电标定时加热电压约6~8V,电流约0.6~0.8A(此项调节应在实验前进行,控制加热功率,使体系在2~3分钟内升高约1度)。记录好通电到断电的加热时间,当体系升温幅度将近溶解降温幅度时,断开电源,但记录仪继续进行,直到温度上升趋势与标定前期相似为止。
5·杜瓦瓶重新装水,在做一次实验。
五·数据处理
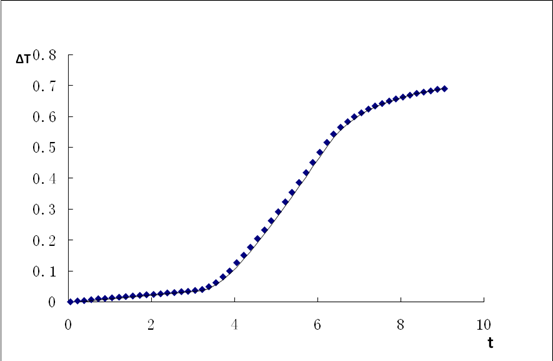
1·用外推法得到溶解过程和标定过程的温差(记录图上表示温差的延长线长度)
溶解过程温差变化图:

电标定过程温差变化:

2·由两次的结果的平均值计算溶解热。
第一次测定;
W=3.3252
I = 1.289
V=6.98
t开始= 3.1
t结束= 6.1
ΔT1 = 0.620
ΔT2 = 0.779
由公式:ΔH=(M/W)IVt(ΔT1/ΔT2)得
ΔH溶解 = 39189.39 J/mol
第二次测定:
W= 3.3108
I = 1.289
V=7.002
t开始= 3.1
t结束= 6.11
ΔT1 = 0.592
ΔT2 = 0.753
由公式: ΔH=(M/W)IVt(ΔT1/ΔT2)得
ΔH溶解 = 39132.51 J/mol
两次求平均值得:ΔH溶解=39160.95J/mol
3·据有关资料,硝酸钾的溶解热在浓度0.073m附近,温度在12.5~25摄氏度,可用下式表示:
ΔH=34.99-0.157(t-25)KJ/mol
从0.146m冲稀到0.073m的冲稀热用下式计算:
ΔH=243-8.4(t-25)KJ/mol
按以上资料讨论实验误差:

六、实验注意事项
1、实验过程中要求I、V值恒定,故应随时注意观察。
2、固体KNO3易吸水,故称量和加样动作应迅速。固体KNO3在实验前务必研磨成粉状,并在110℃烘干。从漏斗加入时要尽量注意均匀加入,不要造成阻塞,也不要时间太长。
3、本实验应保证样品完全溶解,否则需要重做实验。
4、量热器绝热性能与盖上各孔隙密封程度有关,实验过程中要注意盖好,减少热损失。
5、电标定过程断电后,要等待足够长的时间,让加热器的余热完全传给溶液,否则误差会较大。
第二篇:燃烧热的测定_实验报告
燃烧热的测定
【摘要】通过本实验了解氧弹式量热计的结构及各部分作用,掌握氧弹式量热计的使用方法,熟悉贝克曼温度计的调节和使用方法。学会雷诺图解法校正温度改变值。
关键字:氧弹式量热计 贝克曼温度计
雷诺图解法
引言:根据热化学的定义,1mol物质完全氧化时的反应热称作燃烧热。所谓完全氧化。对燃烧产物有明确的规定。如有机化合物中的碳氧化成一氧化碳不能认为完全氧化,只有氧化成二氧化碳才是完全氧化。
量热法是热力学的一种基本实验方法。在恒容或恒压条件下可以分别测得恒容燃烧热Qv和恒压燃烧热Qp。再根据热力学第一定律 Qp=Qv+△n(RT) 换算为恒压燃烧热。另外,直接测量热实际上是几乎不可能的,热量的传递往往表现为温度的改变,故实际中往往采用测量温差的办法来间接测量热。
一、实验目的
1、使用氧弹式量热计测定固体有机物质的恒容燃烧热,并由此求算其摩尔燃烧热。
2、了解氧弹式量热计的结构及各部分作用,掌握氧弹式量热计的使用方法,熟悉贝克曼温度计的调节和使用方法。
3、掌握恒容燃烧热和恒压燃烧热的差异和相互换算。
4、学会雷诺图解法校正温度改变值。 1、燃烧与量热
根据热化学的定义,1mol物质完全氧化时的反应热称作燃烧热。
Qp = Qv + △nRT
2、氧弹热量计
氧弹热量计的基本原理是能量守恒定律。
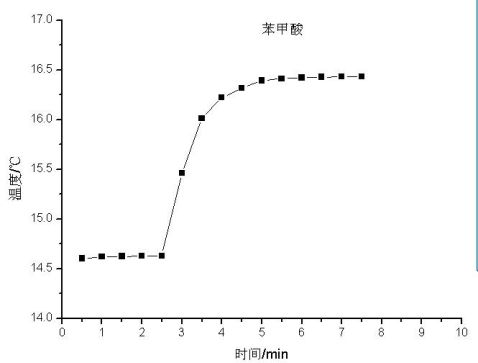
(-m样/M)QV - l〃Ql =(m水C水+C计)△T 3雷诺温度校正图
三、仪器及设备
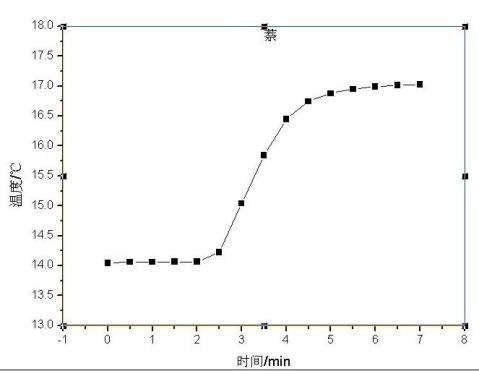
苯甲酸 萘
氧弹式量热计
1-恒热夹套 2-氧弹3-量热容器4-绝热垫片5-隔热盖盖板 6-马达7,10-搅拌器8-伯克曼温度计9-读数放大镜11-振动器12-温度计
四、实验步骤
1、称取苯甲酸约0.9g,压片;

2、把盛有苯甲酸片的坩埚放于氧弹内的坩埚架上,连接好点火丝;
3、盖好氧弹,与减压阀相连,充气到弹内压力为
1.2MPa为止
4、把氧弹放入量热容器中,加入水;
5、接好电路,计时开关指向“1分”,开启电源。约10min后,若温度变化均匀,开始读取温度。读数前5s振动器自动振动,两次振动间隔1min,每次振动结束读数;
6、在第10min读数后按下“点火”开关,同时将计时开关倒向“半分”,点火指示灯亮。加大点火电流使点火指示灯熄灭,样品燃烧。灯灭时读取温度;
7、记录5个数据后,改为1min计时,在记录温度读数至少10min,关闭电源。先取出贝克曼温度计,再取氧弹,旋松放气口排除废气;
8、称量剩余点火丝质量,清洗氧弹内部及坩埚;
9、取萘0.5g压片,重复上述步骤进行实验,记录燃烧过程中温度随时间变化的数据。 五、思考题
1.加入内筒中水的温度为什么要选择比外筒水温低?低多少合适?为什么?
2.在燃烧热测定实验中,哪些是体系?哪些是环境?有无热交换?这些热交换对实验结果有何影响?
3.在燃烧热测定的实验中,哪些因素容易造成实验误差?如何提高实验的准确度?
1、本实验成功的关键是什么?应采取什么措施? 答:点火成功、试样完全燃烧是实验成败关键,可以考虑以下几项技术措施:
①试样应进行磨细、烘干、干燥器恒重等前处理,潮湿样品不易燃烧且有误差;
压片紧实度:一般硬到表面有较细密的光洁度,棱角无粗粒,使能燃烧又不至于引起爆炸性燃烧残剩黑糊等状。
②点火丝与电极接触电阻要尽可能小,注意电极松动和铁丝碰杯短路问题;
③充足氧并保证氧弹不漏氧,保证充分燃烧。燃烧不完全,还时常形
成灰白相间如散棉絮状;
④注意点火前才将二电极插上氧弹再按点火钮,否则因仪器未设互锁功能,极易发生(按搅拌钮或置0时)误点火,样品先已燃烧的事故。
2、燃烧热的测定中样品为什么要压片?
答:排除空气等气体杂质的同时,节省了样品在氧弹
中所占体积,减小误差。同时,压片后的样品燃烧会更充分。
【参考文献】
[1]傅献彩 ,沈文霞 ,姚天扬 .物理化学 [M].北京 :
高等教育出版社 , 2006 : 34285
[2]印永嘉 ,奚正楷 ,李大珍 .物理化学简明教程 [M].北京 :高等教育出版社 , 2007 : 10264
[3]高贵军 .物理化学教学中体现的科学研究规律和方
法 [J ].河北北方学院学报 :自然科学版 , 2003 , 19 (03) : 42244
[4]MustafaS,JudithM,Bennett.Astudyofturkishchem
istryundergraduates’understandingofentropy[J]. JChem Educ, 2007, 84 (07): 120421 207
[ 5 ] William F , Coleman. Luminescent molecular thermometers [J ]. J Chem Educ , 2006 , 83 (05) : 7402741
[6]王存娥 . “燃烧热测定”教学实验的改进 [J ].衡
阳师专学报 :自然科学版 , 1993 , 11 (02) : 80281
[7]张建策 ,毛力新 .燃烧热测定实验的进一步改进
[J ].化工技术与开发 , 2005 , 34 (06) : 43244
[8]李咏梅 ,李人宇 ,夏海涛 ,等.燃烧热测定实验的
绿色化研究 [J ].甘肃科技 , 2008 , 24 (17) : 52253
[9]李森兰,杜巧云 ,王保玉 .燃烧热测定实验研究
[J ].大学化学 , 2001 , 16 (01) : 51257
[10 ] 钟红梅 .氧弹式量热法测定燃烧焓实验的改进
[J ].科技信息 (学术研究 ) , 2008, (15) : 72
[11 ]复旦大学 .物理化学实验 [M].北京 :高等教育出版社 , 1993 : 43248
[12 ]东北师范大学等校编 .物理化学实验 [M].北京 :高等教育出版社 , 1989 : 45249 [责任编辑 :刘守义 ]

