明矾中铝含量的测定
姓名:张昀
?化学系, 化学, 082班, 学号2008121239?
摘要 明矾中铝含量的测定,不宜采用直接滴定法。因为Al3+对二甲酚橙等指示剂有封闭作用,且Al3+与EDTA络合缓慢,需要加过量EDTA并加热煮沸,络合反应才比较完全,且在酸度不高时,Al3+水解生成一系列多核氢氧基络合物,如[Al2(H2O)6(OH)3]3+,[Al3(H2O)6(OH)6]3+等,即使将酸度提高至EDTA滴定Al3+的最高酸度,仍不能避免多核络合物的生成。铝的多核络合物与EDTA络合缓慢,且络合比不恒定,对滴定不利。为避免上述问题,可采用返滴定法。如先加一定量过量的EDTA标准溶液,在pH≈3.5时,煮沸溶液,由于此时酸度较大,故不利于形成多核氢氧基络合物,又因EDTA过量较多,故能使Al3+与EDTA络合完全,络合完全后,调节溶液pH=5左右,(此时AlY稳定,也不会重新水解析出多核络合物),加入指示剂二甲酚橙,再用Zn2+标准溶液进行返滴定。该测定方法简便易行且准确度较高,基本符合实验要求。
关键词 明矾[KAl(SO4)2·12H2O],返滴定法,酸度,二甲酚橙指示剂,铝,EDTA(Y)溶液,六次甲基四胺
1 引言
KAl (SO4)2·12H2O俗称明矾或白矾,是一种无色透明的晶体,其溶液呈弱酸性,常用作净水剂、食品添加剂,在工农业、食品加工业中有着重要的作用。
目前国内外测定食用明矾中铝的含量主要有五种方案:
第一种方案是直接滴定法,即DCTA(环己烷二胺四已酸)在室温下与Al3+迅速定量络合。这种方法操作简便,但所使用的DCTA价格比较昂贵[1]。
第二种方案为置换滴定法:此法用于测定像合金,硅酸盐,水泥和炉渣等复杂试样中铝的含量,以此提高选择性。在pH=3-4时,加入定过量的EDTA溶液煮沸使Al3+与EDTA充分配合,冷却后调PH至5-6,以二甲酚橙为指示剂,用Zn标准溶液滴定过量的EDTA(不记体积)至微红色,然后加入过量的NH4F,加热至沸,使AlY-与F-之间发生置换反应,并释放出与Al3+配合的EDTA,
AlY-+6F-+2H+==== AlF63-+H2Y2
再用Zn2+标准溶液滴定释放出的EDTA至紫红色,即为终点[2]。
第三种方案为返滴定法(Zn2+标准溶液):此法用于简单试样如明矾,氢氧化铝,复方氢氧化铝片,氢氧化铝凝胶等药物中铝含量的测定。由于Al3+易形成一系列多核羟基络合物,这些多核羟基络合物与EDTA络合缓慢,且Al3+对二甲酚橙指示剂有封闭作用,故通常采用返滴定法测定铝。加入定量且过量的EDTA标准溶液,先调节溶液pH至3-4,煮沸几分钟,使A13+与EDTA络合反应完全。冷却后,再调节溶液pH至5-6,以二甲酚橙为指示剂,用Zn2+标准溶液滴定至溶液由黄色变为紫红色,即为终点[3]。
第四种方案为返滴定法(Cu2+标准溶液):向试液中准确加入30.00mL 0.02mol·L-1EDTA溶液,记下VEDTA,加入15mL pH=4.2的HAc-NaAc缓冲溶液,煮沸约1min,取下,稍冷,补加上述缓冲溶液10~15mL,加入两滴1-(2-吡啶偶氮)-2-萘酚(PAN)指示剂,立即用0.02mol·L-1CuSO4标准溶液滴定,至溶液呈紫红色为终点。记下VCuEDTA.终点时温度不低于80℃[4].
第五种方案为重量分析法:精确称取三份明矾试样(2g左右)与250mL的烧杯中,加热溶解烧杯中的明矾试样,直至溶液澄清。调节pH=3~9,往烧杯中滴加0.2mol/L的8-羟基喹啉至过量,此时溶液产生沉淀。
Al3++ 3C9H7ON=Al(C9H6ON)3↓ + 3H+
抽滤分离沉淀,将沉淀定量转入瓷坩埚中,高温灼烧1h后,置于干燥器中冷却。分析天平生恒重至相邻两次质量差为2mg,称得的质量即为Al2O3的质量。计算每克明矾试样中Al2O3的质量,以mg/g表示[5]。
A13++ Y4-= AlY-Zn2++ Y4-= ZnY2-
分析测定中能用滴定法的不采用重量分析法,因为此法误差较大,耗用时间长
比较上述五种方案可知,第三种方案操作简便易行且准确度较高,故本实验采用第三种方案返滴定法:即先调节溶液pH至3-4,加入定过量的EDTA溶液,煮沸;冷却,再调节溶液pH至5-6,以二甲酚橙为指示剂,用Zn2+标准溶液滴定至溶液由黄色变为橙色。
2 实验原理
明矾 KAl(SO4)2·12H2O中Al的测定,可采用EDTA配位滴定法。由于Al3+易形成一系列多核羟基络合物,这些多核羟基络合物与EDTA络合缓慢,且Al3+对二甲酚橙指示剂有封闭作用,故通常采用返滴定法测定铝。加入定量且过量的EDTA标准溶液.先调节溶液pH为3-4,煮沸几分钟,使A13+与EDTA络合反应完全(因为氢氧化铝的溶度积常数KSP=1.3×10-33,当 [AL3+]=0.020mol/L,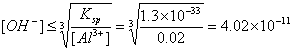 ,则
,则
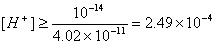 ,所以pH≤3.6,所以调节溶液pH为3~4)。冷却后,再调节溶液pH至5-6{
,所以pH≤3.6,所以调节溶液pH为3~4)。冷却后,再调节溶液pH至5-6{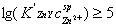 ,
,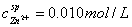 ,故
,故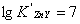 ,则
,则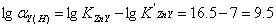 查附录表10,可知最高酸度:pH≈3.5因为氢氧化锌的溶度积常数KSP=10-16.92,则
查附录表10,可知最高酸度:pH≈3.5因为氢氧化锌的溶度积常数KSP=10-16.92,则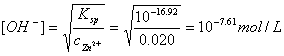 ,pH=14-7.61≈6.4(水解酸度),所以冷却后,再调节溶液pH至5-6,此时AlY稳定,也不会重新水解析出多核络合物},以二甲酚橙为指示剂,用Zn2+标准溶液滴定至溶液由黄色变为橙色:Zn + Y = ZnY,即为终点。有很多金属离子都干扰铝的测定,可根据实际情况采用适合的措施消除干扰。
,pH=14-7.61≈6.4(水解酸度),所以冷却后,再调节溶液pH至5-6,此时AlY稳定,也不会重新水解析出多核络合物},以二甲酚橙为指示剂,用Zn2+标准溶液滴定至溶液由黄色变为橙色:Zn + Y = ZnY,即为终点。有很多金属离子都干扰铝的测定,可根据实际情况采用适合的措施消除干扰。
滴定完毕后:
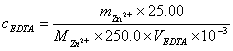
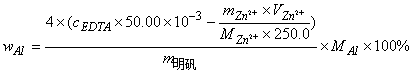
3 实验用品
3.1 仪器
全自动电光分析天平,酸式滴定管?50ml?,电子秤,容量瓶(100 mL 、250mL各一个),锥形瓶(250mL三个),烧杯?50mL、250mL 、500mL?,胶头滴管,玻璃棒,聚乙烯塑料试剂瓶(一个),电炉,量筒(10 mL),移液管?25mL一个?,称量瓶(两个),药匙(两个)
3.2 药品
明矾 [KAl (SO4)2·12H2O] 试样,乙二胺四乙酸二钠盐(Na2H2Y·2H2O),二甲酚橙指示剂(2g/L),六次甲基四胺溶液(20%),盐酸溶液(1:1),ZnSO4·7H2O(s),pH=3.5的缓冲溶液
4 实验步骤
4.1 溶液的配制
4.1.1 0.02mol/LEDTA的配制
用电子秤称取约4.0g固体乙二胺四乙酸二钠盐于500mL的烧杯中,加入200mL蒸馏水并加热使其完全溶解,然后加蒸馏水稀释至500mL。静置冷却后转入聚乙烯塑料试剂瓶中,盖紧瓶塞,摇匀静置备用。(EDTA的Mr=372.44)
4.1.2 0.02mol/L Zn2+标准溶液的配制
准确称取固体ZnSO4·7H2O 1.4~1.5g于250mL的小烧杯中,加水并加热,待完全溶解后用少量水冲洗烧杯内壁,冷却后将溶解液定量转移至250mL容量瓶中,并加水稀释至刻度,摇匀静置备用。计算所配制的Zn2+标准溶液的准确浓度。
4.2 EDTA标准溶液的标定
用移液管准确移取25.00 mL Zn2+标准溶液于锥形瓶中,加盐酸溶液(1:1)约2mL,使pH≈3.5,加2~3d二甲酚橙指示剂(2g/L),滴加20%六次甲基四胺溶液至溶液呈现稳定的紫红色后再多加5mL六次甲基四胺。用EDTA溶液滴定,当溶液由紫红色恰好转变为黄色且半分钟内不退色时,即为终点。记下此时所用EDTA的体积,并计算EDTA标准溶液的准确浓度,重复以上操作,平行测定三次,其相对平均偏差须在0.3%以内。
4.3 明矾试样的测定
准确秤取明矾试样[KAl(SO4)2·12H2O,Mr=474.41]0.94~0.95g于50mL小烧杯中,加热使其完全溶解,待冷却后将溶液定量转移至100mL容量瓶中,用蒸馏水稀释至刻度,摇匀静置备用。
用移液管准确移取25.00mL明矾试样标准溶液置于250mL锥形瓶中,用滴定管准确量取EDTA标准溶液50.00mL于锥星瓶中,然后加入10mLpH=3.5的缓冲溶液,在水浴箱上加热煮沸近3min,然后放置冷却至室温。
在锥形瓶中加入六次甲基四胺5mL,二甲酚橙指示剂3~ 4滴,用Zn2+标准溶液返滴定至溶液由黄色变为橙色且半分钟内不退色时,即为终点。
根据所消耗的Zn2+标准溶液体积,计算所测明矾中的铝含量。重复以上操作,平行测定3 次,控制相对平均偏差在0.3%以内。
5 实验记录及数据处
5.1 0.02mol/L Zn2+标准溶液的配制

5.2 0.02mol/LEDTA标准溶液的标定

5.3 明矾试样中铝含量的测定
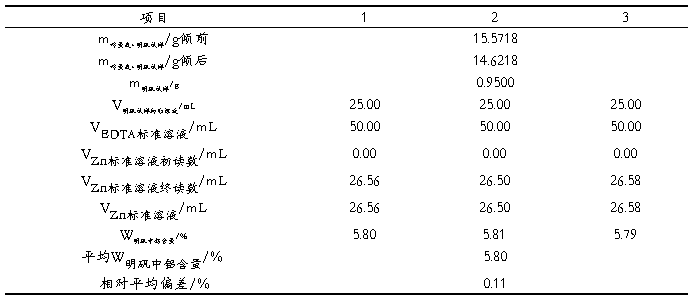
6 实验结果与讨论
6.1 测定结果
本实验采用返滴定法测定明矾中铝的含量,其中所配制的Zn2+标准溶液的浓度0.02000mol/L ;所标定EDTA的标准浓度为0.02083mol/L,明矾中铝的含量为 5.80% 。
6.2 误差分析
6.2.1 分析天平仪器老化,灵敏度不高,有系统误差;
6.2.2 滴定过程中,有少量溶液滞留在锥形瓶内壁,未用蒸馏水完全冲入溶液中,导致误差;
6.2.3 滴定终点指示剂颜色判断有误,造成随机误差。
6.3 注意事项
6.3.1 注意各步中pH值的控制
6.3.2 在明矾试样的测定中,当pH<6时,游离的二甲酚橙显黄色,滴定至Zn2+稍微过量时Zn2+与部分二甲酚橙生成紫红色配合物,黄色与紫红色混合呈橙色,故终点颜色为橙色。
6.3.3 注意滴定时指示剂的用量,及滴定终点颜色的正确判断;
6.3.4 注意滴定时的正确操作:滴定成线,逐滴滴入,半滴滴入。
6.4 心得体会
通过本次设计性实验,我学会了用返滴定法测定明矾中铝的含量,熟练掌握了通过控制酸度而使金属离子与EDTA形成稳定的络合物,提高了独立思考和查阅资料的能力,更加熟练的掌握了滴定管、移液管、全自动电光分析天平的使用。
参考文献
[1] 华中师范大学等,分析化学 上册[M],北京:高等教育出版社,2001,192
[2] 吴俊方,工科化学基本实验[M],南京:东南大学出版社,2006,94
[3] 武汉大学,吉林大学,中山大学,中国科学技术大学.分析化学实验(第五版)[M].北京:高等教育出版社,2001,209
[4] 蔡明招,分析化学实验[M],北京:化学工业出版社,2004,55
[5] 鲍浩波,分析化学,武汉大学(第五版),306
[6]http://jc2.ecjtu.jx.cn/huaxue/te/Read.News.asp?News.ID=573
Aluminum alum Determination
Zhang yun
(Class082 Learning number2008121239)
The summaryAlum in the determination of aluminum, not by direct titration. Al3 +because of the XO, and other indicators have closed, and Al3 + and EDTA complex slow, the need to increase heat and boil over EDTA, the reaction is rather complex fully, and when the acidity is not high, Al3 +hydrolysis generation A series of multi-hydrogen complexes, such as [Al2(H2O)6(OH)3]3+、[Al3(H2O)6(OH)6]3 +and so on, even if the acidity will be increased to EDTA Titration of Al3 +The maximum acidity, can not avoid the generation of complex multi-core. The aluminum complex and multi-EDTA complex slow and complex than a constant, the titration of the negative. To avoid these problems could be back titration. If the first increase in over a certain amount of EDTA standard solution in the pH ≈ 3.5, the solution to boil, due to higher acidity at this time, it is not conducive to the formation of hydrogen-based multi-core complex, due to the excess EDTA more, it can Al3 +EDTA complex and completely, totally complex, conditioning solution pH = 5 or so (at this time AlY stability, and will not re-analysis of water out of complex multi-core), the indicator to join XO, and then Zn2 +Standard solution for back titration. The method is user-friendly and high accuracy, in line with the basic requirements of the experiment.
Key wordsAlum [KAl (SO4)2? 12H2O], back titration, acidity, XO indicator, aluminum, EDTA (Y) solution, hexamine
第二篇:明矾净水实验的问题在哪里


