目前位置:首页—>羧酸及其衍生物—>K2羧酸及其衍生物的物理性质
羧酸及其衍生物的物理性质
教学目标:
1.了解羧酸一般物理性质及其影响因素。
2.掌握羧酸及其衍生物 IR 特征。
教学重点:IR特征
教学安排:B5, K1—>K2;10min
一、一般物理性质
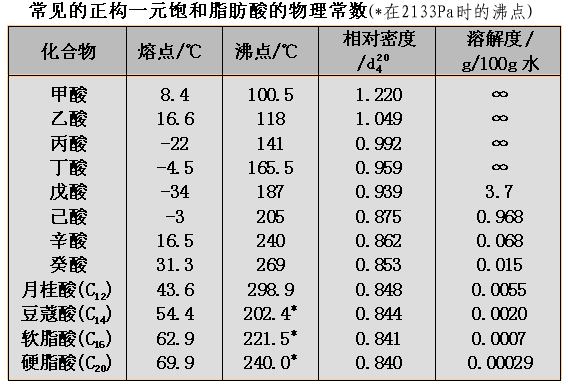
低级的一元羧酸(C1-C9)是液体,C1-C3的羧酸有一定挥发性,并且有较强的刺激性;C4-C9的羧酸不同程度地具有腐败气味,并且是具有一定粘度的油状液体。C10以上的羧酸则是石蜡状固体,气味很小。二元羧酸以及芳香族羧酸都是晶体。
羧酸的沸点较分子量相近的醇高,这是由于羧基的强极性和分子间的氢键所致。在气态时,甲酸、乙酸等是以双分子缔合形态出现。与烷烃相似,偶数碳原子的羧酸其熔点要比与之相邻的奇数碳原子羧酸的熔点高。
C1-C4的正构羧酸由于分子的极性大,与水分子可很好地形成氢键,所以它们的溶解度很大;但正戊酸在水中的溶解度只有3.7g/100g水。高级的一元酸在水中的溶解度非常小,甚至不溶于水。常见的二元酸在水中都有很好的溶解度。
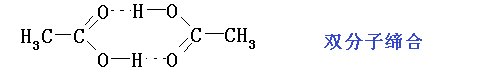
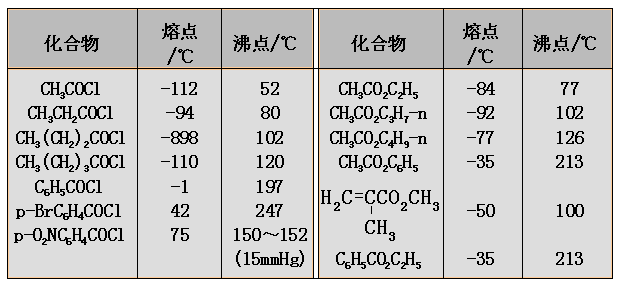
酰氯、酸酐和酯的沸点与分子量相近的醛酮大体相近,酰胺由于分子间可形成氢键,而具有很高的沸点。低级的酯和酰胺在水中有一定的溶解度;但低级的酰氯和酸酐在水中容易发生水解。一般情况下,酰氯和酯的熔点比较低,酰胺的熔点较高,不同的酸酐的熔点变化是较大的。
低级的酰氯和酸酐都有刺鼻气味,而低级的酯却有芳香气味并可用作香料;低级的酰胺是良好的非质子型极性溶剂。常见的羧酸及其衍生物在一般的有机溶剂中有良好的溶解性。
一些常见的羧酸衍生物的熔点和沸点如下表:
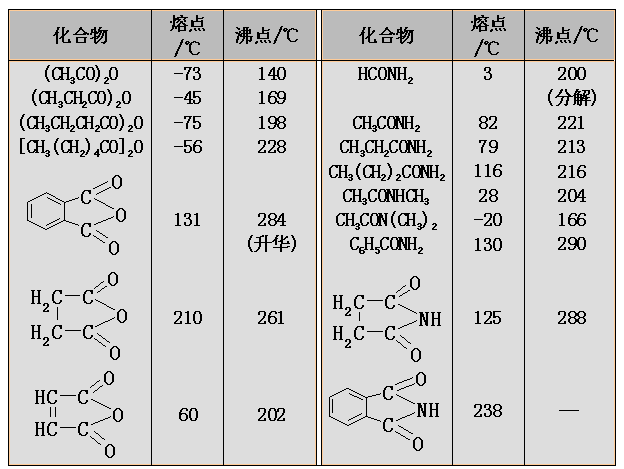
二、光波谱性质
由于羧酸分子的羟基之间可形成氢键,在 3300cm-1处有非常强而宽的羟基的特征峰,并且该峰可含盖烃基中的 CH3和 CH2的 C-H 键伸缩振动吸收峰的区域;在 2500-2700cm-1处,还有 O-H 键的伸缩振动。另外,OH 的弯曲摆动(面外摇摆)在 925cm-1处有一个比较宽的特征吸收峰。脂肪族羧酸中的羰基在 1700-1725cm-1处有中等强度的吸收,而芳香族羧酸的羰基在 1680-1700cm-1处有吸收。在羧酸的各种衍生物中,羰基在红外光谱中出现吸收的位置是不同的,羰基越缺电子,吸收波数越高;羧酸根据负离子的红外吸收波数是最低的。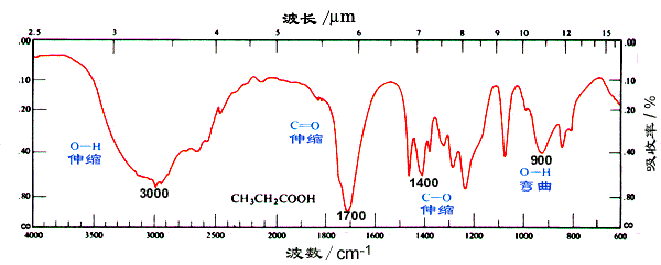
丙酸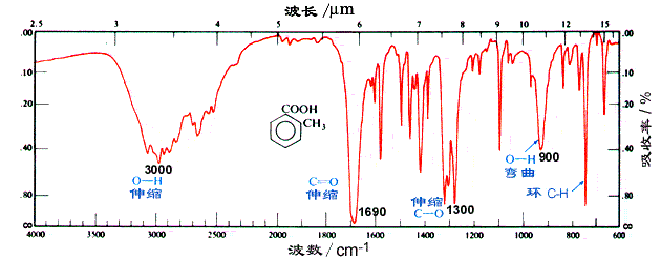
邻甲苯甲酸
邻甲苯甲酰氯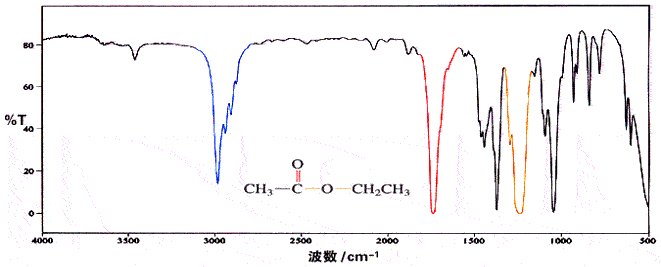
乙酸乙酯
邻甲苯甲酰氯
乙酸乙酯
x羰基的影响下,其化学位移多在δ=2.2-2.5。
三、关键词
羧酸的物理性质、羧酸的光波谱性质
第二篇:烃的衍生物第三单元羧酸的性质和应用
烃的衍生物第三单元羧酸的性质和应用
【学习目标】
1.通过对乙酸性质的探究活动,了解羧酸具有酸性的原因,认识酯化反应的特点。
2.认识甲酸的性质
【教学的重点和难点】
乙酸的性质,甲酸的性质
【复习提问】乙醛能够用被氧气氧化成乙酸,写出反应的化学化学方程式
所得有机物为它的官能团是,含有该官能团的一类物质我们称之为。
一、羧酸的概念及结构
1、概念:
2、官能团:
3、分类:
(1)根据烃基不同可分为:
(2)根据羧基数目不同可分为:
(3)根据烃基中碳原子数目多少可分为:
4、饱和一元羧酸的分子通式为:
5、乙酸的分子式结构式结构简式
二、羧酸的物理性质:
1、乙酸的物理性质:
乙酸俗称,为色体,有强烈的气味,易溶于,0℃时,乙酸凝结成冰一样的物质,所以纯净的乙酸又叫做。
2、饱和一元羧酸的物理性质:
随碳原子数增多,熔沸点升高,在水中的溶解度降低,C1~C4的羧酸能与水互溶,(酸性减弱)。
三、羧酸的化学性质:
1、酸的通性:
乙酸可以使湿润的蓝色石蕊试纸
用方程式表示下列过程:
① 乙酸在水中电离:
② 与金属钠的反应:
比较乙酸,乙醇,苯酚,水与金属钠反应的剧烈程度,分析原因:
③ 与氧化铜的反应:
④ 与NaOH的反应:
⑤ 与碳酸钠的反应:
比较乙酸,碳酸,苯酚的酸性强弱:
2、酯化反应:
乙酸乙酯的生成:
反应方程式:
反应特点:
根据乙酸与乙醇酯化反应的原理,对比乙酸乙酯发生水解时的共价键断裂的情况,两者之间有何联系?
【练习】:完成下列酯化反应:
(1)CH3COOH + CH2OH

CH2OH
(2) COOH
 + CH3CH2OH
+ CH3CH2OH
COOH
(3) CH2OH
 + HNO3
+ HNO3
CHOH

CH2OH

 (4) COOH + CH2OH
(4) COOH + CH2OH
COOH CH2OH
(5) 2 CH3CHCOOH

OH
 (6)CH2CH2CH2COOH
(6)CH2CH2CH2COOH
OH
3、缩聚反应:
通过酯化反应,可以得到高分子化合物,如聚对苯二甲酸乙二酯的生成
比较加聚反应与缩聚反应的区别:
【练习】:对苯二甲酸和1,4-丁二醇作用生成高分子酯
四、甲酸的结构和性质:
甲酸俗称,分子式为,结构式,结构简式,甲酸中既有
,又有。
【问题解决】根据甲酸的结构预测它可能具有的性质。归纳整理。
【课后巩固】:
1.某有机物既能被氧化,又能被还原,且氧化后与还原后的产物能发生酯化反应,所生成的酯又能发生银镜反应,则该有机物是 ( )
A.CH3OH B.HCHO C.HCOOH D.CH3CH2CHO
2.在下列物质中,既能使溴水褪色,又能使酸性高锰酸钾溶液褪色,还能使紫色石蕊试液变为红色的是 ( )
A.苯 B.苯酚 C.丙烯酸 D.甲酸甲酯
3.只用水就能鉴别的一组物质是 ( )
A.苯、乙酸、四氯化碳 B乙醇、乙醛、乙酸
C.乙醛、乙二醇、硝基苯 D.苯酚、乙醇、甘油
4.用括号内的试剂和分离方法,除去下列物质中的少量杂质,正确的是 ( )
A.乙酸乙酯中的乙酸(饱和Na2CO3溶液,分液)
B.苯中的甲苯(溴水,分液)
C.溴苯中的溴(KI溶液,分液)
D.乙醇中的乙酸(NaOH,蒸馏)
5.重氮甲烷(CH2N2)能与酸性物质反应:R-COOH+CH2N2→R-COOCH3+N2。下列物质中能与重氮甲烷反应但产物不是酯的是 ( )
A.H-CHO B.C6H5OH C.C6H5CH2OH D.C6H5COOH
6.某物质中可能有甲醇、甲酸、乙醇、甲酸乙酯几种物质中的一种或几种,在鉴定时有下列现象:①有银镜反应 ②加入新制Cu(OH)2悬浊液,沉淀不溶解 ③与含有酚酞的氢氧化钠溶液共热时发现溶液中红色逐渐变浅至无色,下列叙述中正确的是 ( )
A.有甲酸乙酯和甲酸 B.有甲酸乙酯和乙醇
C.有甲酸乙酯,可能有甲醇 D.几种物质都有
7.以乙醇为原料,用下述6种类型的反应:①氧化;②消去;③加成;④酯化;⑤水解;⑥加聚,来合成环乙二酸乙二酯()的正确顺序是 ( )
A.①⑤②③④ B.①②③④⑤ C.②③⑤①④ D.②③⑤①⑥
8. 胆固醇是人体必需的生物活性物质,分子式为C27H46O。一种胆固醇酯是液晶材料,分子式为C34H50O2。生成胆固醇的酸是:( )
A.C6H50O2B.C6H5COOH C.C7H15COOH D.C6H5CH2COOH
9 .有A、B、C、D、E五种有机物,分别由碳、氢两种元素或碳、氢、氧三种元素组成。五种有机物各取0.1mol,分别完全燃烧,都能得到4.48L(标准状况下)二氧化碳。
(1) A氧化能得到B,E氧化能得到A;
(2) D在一定条件下跟水反应能得到E,D跟氢气加成得到C;
(3) B易溶于水,水溶液呈酸性。
则这五种有机物的结构简式分别为:A___________,B___________,C___________,D___________,E___________。
10.酸牛奶中含乳酸,
⑴乳酸跟足量金属钠反应的化学方程式;
⑵乳酸与少量碳酸钠溶液反应的化学方程式:;
⑶乳酸在浓硫酸存在下,两分子相互反应生成链状化合物的化学方程式
;
⑷乳酸在浓硫酸存在下,两分子相互反应生成环状化合物的化学方程式
;
⑸乳酸在浓硫酸条件下,分子内脱水且脱水后的产物能使溴水褪色,则此产物的结构简式为
⑹乳酸在浓硫酸条件下,分子内脱水且脱水后的产物不能使溴水褪色,则此产物的结构简式为
 11.分子式为C13H16O2的惕各酸苯乙酯广泛用于香精的调香剂。已知:
11.分子式为C13H16O2的惕各酸苯乙酯广泛用于香精的调香剂。已知:
为了合成该物,某实验室的科技人员设计
了下列合成路线:
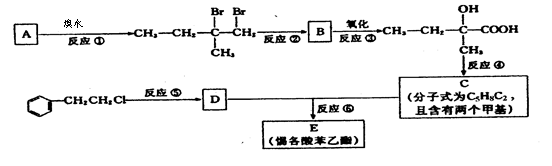
试回答下列问题:
(1)试写出:A的结构简式;B的结构简式。
(2)反应②中另加的试剂是;反应④的一般条件是。
(3)试写出反应生成E的化学方程式:。
(4)上述合成路线中属于取代反应的是(填编号)。

