20##年高一化学第一次月考测试题
姓名班级2014.10.10
相对原子质量:H 1 He 4 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32
Cu 64 Zn 65 Cl 35.5 K 39 Ca 40 P 31
Zn 65 Cl 35.5 K 39 Ca 40 P 31
一、选择题(每小题4分,共60分。每小题只有一个选项符合题意,请将它填到答题栏内)
下列物质与常用危险化学品的类别不对应的是( )
A.H2SO4、NaOH——腐蚀品 B.CH4——易燃液体
C.Na——遇湿易燃物品 D.KMnO4、K2Cr2O7——氧化剂
2.为了除去粗盐中的Ca2+、Mg2+、SO及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序可以是( )
A.⑤②④③① B.④①②⑤③
C.②⑤④①③ D.①④②⑤③
3.下列实验操作中错误的是( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,萃取剂与原溶剂要互不相溶
4.现有三组溶液:①汽油和氯化钠溶液、②39%的乙醇溶液、③碘水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
5.丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g·mL-1,沸点约为55 ℃,分离水和丙酮时最合理的方法是( )
A.蒸发 B.分液 C.过滤 D.蒸馏
6.下列每组中的两种物质,能用分液漏斗分离且油层由分液漏斗下口倒出的是( )
A.四氯化碳和水 B.苯和水
C.芝麻油和水 D.酒精和水
6.下列实验操作中:①过滤;②蒸发;③溶解;④取液体试剂;⑤取固体试剂。一定要用到玻璃棒的是( )
A、①②③ B、④⑤ C、①④ D、①③⑤
7.某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中( )
A、一定有SO42-B、可能有SO42-或Ag+C、一定无Ag+D、还可能有CO32-
8.如果已知100个氧分子质量为m克,那么阿伏加德罗常数的值是 ( )
A、3200/m B、32/(100m) C、3200m D、m/3200
D、m/3200
9.下列物质中,摩尔质量最大的是( )
A、10 mL H2O B、0.8 mol H2SO4C、54 g Al D、1g CaCO3
10.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A、64g SO2含有氧原子数为1NA
B、物质的量浓度为0 .5mol/L Mg Cl2溶液,含有Cl—离子数为1NA
.5mol/L Mg Cl2溶液,含有Cl—离子数为1NA
C、0.5NA个O2的质量为32g
D、常温常压下,14g N2含有分子数为0.5NA
11. 下列叙述中,正确的是( )
A、在标准状况下,1mol任何物质的体积为22.4L
B、等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等
C、1molH2和1molHe中,所含的分子数相同、原子数相同、质量也相同
D、体积为6L的O2,其质量可能为8g
12.对于质量相同的CH4和O2,下列说法正确的是 ( )
A、所含分子个数相等 B、物质的量相等
C、所含原子个数之比为5:1 D、体积之比为2:1
13.下列数量的各物质所含原子总数按由大到小顺序排列的是( )
①0.5mol氨气 ②标况下22.4L氦气 ③4℃时9mL水 ④0.2mol磷酸
A、①④③② B、④③②① C、②③④① D、①②④③
14.两个体积相同的容器,一个盛有NO,另一个盛有N2和O2(其物质的量之比为1:1),下列关于在同温同压下两容器内的气体的说法中不正确的是( )
A、原子总数相同 B、物质的量相同 C、分子总数相同 D、质量相同
15.在VL硫酸铝溶液中,含有WgAl3+离子,这种溶液中SO42-的物质的量浓度是( )
A、W/27V mol/L B、W/54 mol/L C、W/18V mol/L D、3W/54mol/L
二、非选择题部分(每个空2分,共20分)
16.选择下列实验方法分离物质,将分离方法的字母序号填在横线上。
A.过滤法 B.分液法
C.蒸馏法 D.结晶法
(1)________分离水和豆油的混合物;
(2)________从含有硝酸钾和少量氯化钾的混合溶液中获得硝酸钾;
(3)________分离饱和食盐水和沙子的混合物;
(4)________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃),已知四氯化碳和甲苯互溶。
17.标准状况下,67.2L CO2的质量为___________g,其中含有___________mol氧原子。
18.32gSO2中含分子数为NA,含S原子数目为NA,。
19.200ml 5mol/lNaOH溶液中含溶质的质量是g,取出20 ml溶液,取出的溶液中溶质的物质的量浓度是。
三.实验题(每个空2分,共20分)
20.某同学用18mol/L的浓硫酸配制250mL 0.9mol/L的稀硫酸,并进行有关实验.请回答下列问题:
(1)需要量取浓硫酸mL.
(2)配制该稀硫酸时使用的仪器除量筒、烧杯、外,还必须用到的仪器有、、等.
(3)在配制过程中,若定容时俯视刻度线,则所得溶液浓度0.9mol?L-1(填“大于”、“等于”或“小于”).若没洗涤,则所得溶液浓度0.9mol?L-1(填“大于”、“等于”或“小于”).若容量瓶事先有水没干燥,则所得溶液浓度0.9mol?L-1(填“大于”、“等于”或“小于”).
(4)如何进行定容操作
(5)倒立摇匀后发现液面下降,在补加点水,可以吗。
(6)从配得的溶液中取出20ml,取出的溶液中含溶质的质量是。


16 B D A C 17.132g 6mol 18 0.5 0.5 19 40g 5 mol?L-1
20、(1)12.5mL.
(2)胶头滴管、玻璃棒,250 mL容量瓶等.
(3)大于0.9mol?L-1.
(4)眼睛平视刻线,最后一滴滴入使溶液凹面与刻线相切,即定容结束
(5)不可以
(6)0.018 mol/L.
第二篇:高一化学第一次月考化学测试题
高一化学下学期第一次月考化学测试题(理普)
本试卷第一部分为选择题,第二部分为非选择题
满分为100分,考试时间90分钟。
(需要用到的相对原子质量:H:1 ,C:12 ,O:16 ,Ca:40) 第一部分 选择题(共56分)
一、选择题(每小题2分,每题只有一个正确答案,共40分)
1、下列关于18 8O的叙述错误的是( )
A、质子数为8 B、中子数为8 C、电子数为8 D、质量数为18
2、原子序数从11—17的元素,随着原子序数的递增而依次减小的是( )
A、电子层数 B、最外层电子数 C、原子半径 D、最高正价
3、下列物质碱性最强的是( )
A、NaOH B、Al(OH) 3 C、Ca(OH)2 D、KOH
4、下列各组元素中,以金属性逐渐减弱的顺序排列的是( )
A、Li、K、Na B、Na、Mg、Al C、Ca、K、Cs D、Ca、Mg、Na
5、下列电子式书写正确的是( )
6、某元素二价阳离子的核外有18个电子,质量数为40,该元素的原子核内中子数为( )
A、16 B、18 C、20 D、22
7、元素X原子最外层有6个电子,元素Y原子最外层有3个电子,这两种元素形成的化合物的化学式可能为( )
A、XY2 B、X2Y C、Y3X2 D、Y2X3
8、下列物质性质比较正确的是( )
A、酸性:H2SO4 > HClO4 > H3PO4
B、碱性:NaOH > KOH > RbOH
C、非金属性:P > S > Cl
D、气态氢化物稳定性:HF >HCl >H2S
9、下列说法不符合ⅦA族元素性质特征的是( )
A、它们的最高正价都为 +7价 B、从上到下原子半径逐渐减小
C、从上到下非金属性逐渐减弱 D、从上到下氢化物的稳定性逐渐增强
10、下列说法正确的是( )
A、F、Cl、O、N都是第二周期的元素
B、周期表中的第一纵行都是金属元素
C、原子的最外层有两个电子的元素都排在第ⅡA族
D、第三周期元素的原子核外都有三个电子层
11、下列各组物质中,互为同位素的是( )
A、水和重水 B、石墨和金刚石 C、氕和氘 D、纯碱和烧碱
12、某元素的最高价氧化物对应的水化物化学式为H2XO3,这种元素的气态氢化物的化学式为( )
A、HX B、H2X C、XH3 D、XH4
13、元素X、Y可以组成化学式为XY2的共价化合物,则X、Y可能为( )
A、ⅠA 和 ⅦA B、ⅡA 和 ⅥA C、ⅣA 和 ⅥA D、ⅠA 和 ⅤA
14、现有A、B两种原子,已知A原子的核外电子总数是B原子核外电子总数的1/2倍,B原子的L层电子数为A原子L层电子数的2倍,A和B分别为( )
A、C和Mg B、B和He C、Cl和C D、Be和O 15、1 mol 某金属A与足量的盐酸反应,放出22.4 L 的H2(标准状况下),并转化为具有Ar原子的电子层结构的离子,则A元素在周期表中的位置为( )
A、第三周期第ⅠA族 B、第四周期第ⅠA族
C、第三周期第ⅡA 族 D、第四周期第ⅡA族
16、X+和Y-具有相同的电子层结构,下列说法正确的是( )
A、原子序数: X<Y B、原子半径:X<Y
C、离子半径: X+>Y- D、原子最外层电子数:X<Y
17、某元原子素最外层只有1个电子,它与卤素相结合时,形成的化学键( )
A、一定是共价键 B、一定是离子键
C、可能是共价键,也可能是离子键 D、以上说法都不正确
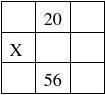
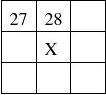
18、下列各图为元素周期表的一部分,表中的数字为原子序数,其中X为37
的是( )
A B C D
19、同周期的X、Y、Z三种元素,它们最高价氧化物对应的水化物分别为HXO4、H2YO4、H3ZO4 ,则下列判断正确的是( ) A、最高价含氧酸的酸性:H3ZO4 > HXO4 > H2YO4 B、非金属性: X > Y > Z
C、气态氢化物的稳定性按X、Y、Z的顺序依次增强 D、原子半径按Z、Y、X的顺序依次增大
20、短周期元素A、B、C、、的位置如图所示,已知 B、C两元素原子的最外层电子数之和是A元素原子 的2倍,B、C两元素的原子序数之和是A元素的4倍, 则A、B、C依次是( )
A:Be、Na、Al B:B、Mg、Si C:O、P、Cl D:C、Al、P 第二部分 非选择题(共61分)
21、(8分)(用序号填空)下列四种物质中① Ar ② CO2 ③ NaCl ④ KOH ,只存在共价键的是 ,只存在离子键的是 ,既存在离子键又存在共价键的是 22、(20分)用“>”或“<”填空:
(1)酸性:H2CO3 H2SiO3 ; H2SO4 H3PO4; (2)碱性:KOH Ca(OH)2 ; NaOH Mg(OH)2 (3)气态氢化物的稳定性:H2O H2S , H2S HCl (4)通过以上结论可以归纳出:
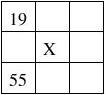
①元素的非金属性越强,其对应的最高价氧化物的水化物酸性越 , ②元素的金属性越强,其对应的最高价氧化物的水化物碱性越 , ③元素的 性越强,其对应其气态氢化物的稳定性越 。 23、(18分)下表为元素周期表的一部分,请用相关元素符号或化学式回答

有关问题:
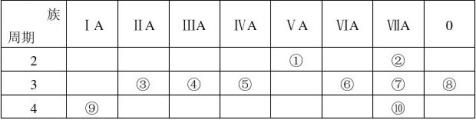
(1)写出⑧和⑨的原子结构示意图: 和 。 (2)比较②、③、④的原子半径由大到小的顺序是 。 (3)在①到⑩元素中最活泼的金属是 ,非金属性最强的元素是 。
(4)表中能形成两性氢氧化物的元素是 ,分别写出该元素的氢氧化物与⑥、⑦最高价氧化物的水化物反应的化学方程式:
(5)请设计一个实验方案,比较⑦和⑩单质的氧化性强弱:
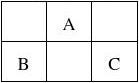
24、(14分)如右图所示,已知 A、B、C、D、E都为短周期元素, A元素的最高价氧化物的化学式为RO2,且R的 气态氢化物中H的质量分数为25%,试回答下列 问题:(用元素符号或化学式回答) (1)写出它们的元素符号:
A ,,
(2)C、D、B形成的气态氢化物稳定性由强到弱的排列顺序是:
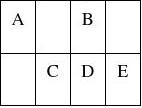
(3)C、D、E三中元素最高价氧化物对应的水化物酸性由强到弱的顺序是: 。
高一化学下学期第一次月考化学测试题(理普)
答 题 卡
分数:
一、 选择题(每小题2分,每题只有一个正确答案,共40分)

二、 非选择题(共60分)
21、 、 、 、
22、(1) 、
(2) 、
(3) 、
(4)① 、②
③ 、
23、(1) 、
(2)
(3) 、
(4) (5) 24、 (1)A ,B ,C ,D ,E ; (2) (3)


